Выход - надсерная кислота
Cтраница 1
Выход надсерной кислоты в значительной степени зависит от плотности тока на аноде и температуры. [1]
Эти побочные реакции снижают выход надсерной кислоты по току. [2]
В табл. VI-1 приведены данные, характеризующие выход надсерной кислоты по току в зависимости от продолжительности электролиза. [3]
 |
Влияние содержания H2SO5 на выход по току H2S208 при различной продолжительности электролиза. [4] |
Присутствие в электролите сернокислых солей аммония, калия, алюминия и других значительно увеличивает выход надсерной кислоты по току. [5]
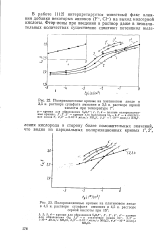 |
Поляризационные кривые на платиновом аноде в 3 5 н. растворе сульфата аммония и 3 5 н. растворе серной.| Поляризационные кривые на платиновом аноде. [6] |
В работе [112] интерпретируется известный факт влияния добавки некоторых анионов ( F -, Cl -) на выход надсерной кислоты. [7]
В работе [ 1911 интерпретируется известный факт влияния добавки некоторых анионов ( F, С1 -) на выход надсерной кислоты. В то же время парциальная поляризационная кривая, соответствующая образованию надсерной кислоты при введении анионов остается неизменной. [8]
Из табл. 1 следует, что при малых содержаниях платины в сплаве, соответствующих а-твердым растворам, и низких температурах ( - 30) выход надсерной кислоты достаточно высок и приближается к значениям, полученным на платиновых анодах. [9]
Из этих данных следует, что при малых содержаниях платины в сплаве, соответствующих а-твердым растворам, и низких температурах ( - 30 С) выход надсерной кислоты достаточно высок и приближается к выходам, получаемым на платиновых анодах. [10]
Значение реакции ( 1) для образования падсерпой кислоты заключается в том, что разряжающийся кислород повышает потенциал платинового анода, благодаря чему значительно ускоряется реакция ( 26) и повышается выход надсерной кислоты. Так как окисление сульфатного иона происходит труднее, чем процесс выделения кислорода по уравнению ( 1), то образование надсерной кислоты постоянно сопровождается выделением Ог, который всегда содержит небольшую примесь озона. Благодаря тому, что [ 1 сильной серной КУслоте концентрация гидроксильных ионов мала, выделение кислорода происходит в допустимых пределах. [11]
Образование ее нежелательно не только потому, что при разложении мононадсернои кислоты выделяется кислород, но и потому, что при этом происходит деполяризация анода. Снижение же потенциала анода приводит к уменьшению выхода надсерной кислоты. Количество мононадсернои кислоты увеличивается с повышением содержания HaSaOg, поэтому последняя может накапливаться лишь до определенного предела. Затем электролит подвергают гидролизу для выделения перекиси водорода, которую отгоняют и улавливают, а кубовый остаток возвращают на электролиз. Из этого следует, что содержание мононадсернои кислоты по сравнению с концентрацией надсерной кислоты необходимо поддерживать возможно более низким. Это обеспечивается увеличением плотности тока, благоприятствующим процессу образования надсерной кислоты. Содержание мононадсернои кислоты можно снизить также путем добавления к электролиту небольших количеств соляной или сернистой кислот, способствующих ее разложению. [12]
Из всех получающихся при электролизе серной кислоты пере-1 кисных соединений - монопадссрная кислота наименее усгойчива, почему образование ее и должно быть по возможности подавлено. Мононадсерная кислота вредна не только потому, что при своем разложении она вызывает потери активного кислорода, но и потому, что она оказывает деполяризующее действие на платиновый: нод. Снижение же потенциала также приводит к уменьшению выхода надсерной кислоты. Потери кислорода находятся в прямой зависимости от содержания мононадсерной кислоты в электролите. Замечательно то, что уже относительно малые количества шшонадсерпой кислоты вызывают значительное уменьшение выхода надсерной кислоты. [13]
Отсюда совершенно необходимо, чтобы разложение по уравнению ( 3), являющееся следствием гидролиза надсерной кислоты до мононадссрной по уравнению ( 4), было бы по возможности устранено. Это может быть достигнуто выбором соответствующих условий процесса электролиза. Необходимо следить, чтобы при электролизе преобладали реакции ( 1), ( 2а) и ( 26), способствующие образованию надсерной кислоты, скорость же реакций от ( 3) до ( 7), протекающих как в электролите, так и на аноде и приводящих к уменьшению выхода надсерной кислоты, была бы по возможности мала. [14]
Скорость процесса гидролиза надсерной кислоты зависит не только от температуры электролита, но и от концентрации серной кислоты. Действительно, скорость гидролиза при этом падает, но уменьшается и выход надсерной кислоты. Последнее обусловлено возрастанием выхода кислорода, образующегося за счет побочной электрохимической реакции окисления воды. [15]
Страницы: 1 2