Выход - 2-нафтол
Cтраница 1
Выход 2-нафтола составляет 65 - 67 % от теоретического, считая на нафталин. [1]
Выход 2-нафтола в промышленности ФРГ составляет 75 % от теоретического ( в расчете а нафталин), в США выход 2-нафтола составляет 74 % от теоретического в расчете на нафталин и 84 % в расчете а бета-соль. [2]
Выход 2-нафтола в промышленности ФРГ составляет 75 % от теоретического ( в расчете а нафталин), в США выход 2-нафтола составляет 74 % от теоретического в расчете на нафталин и 84 % в расчете а бета-соль. [3]
В патентной литературе упоминается о получении 2-нафтола прямым окислением нафталина102, однако о работе опытных установок по этому способу сведения отсутствуют. Известны также английские патенты103 на получение 2-нафтола нагреванием гидроперекиси 2-изапропилнафталина с 50 % - ной серной кислотой ( выход 2-нафтола 92 5 % от теоретического, выход ацетона - 79 5 %), а также окислением 2-метилнафтал на в 2 - афтилметиЛ ГИДропере ись с последующим расщеплением ее на 2-нафтол и формальдегид. Соответствующие гидроперекиси получают окислением ароматических углеводородов кислородом в жидкой фазе в присутствии ди-грег-бутилперекиси или другой органической перекиси. Сведений о практическом применении этих способов не имеется. [4]
В патентной литературе упоминается о получении 2-нафтола прямым окислением нафталина102, однако о работе опытных установок по этому способу сведения отсутствуют. Известны также английские патенты103 на получение 2 - 1наф тола нагреванием гидроперекиси 2-изопро пилнафталина с 50 % - ной серной кислотой ( выход 2-нафтола 92 6 % от теоретического, выход ацетона - 79 5 %), а также окислением 2-метил нафталина в 2-нафтилметилгидроперекиеь с последующим расщеплением ее на 2-нафтол и формальдегид. Соответствующие гидроперекиси получают окислением ароматических углеводородов кислородом в жидкой фазе в присутствии ди-грет-бутилперекиси или другой органической перекиси. Сведений о / практическом применений этих способов не имеется. [5]
 |
Схема щелочного плавления бета-соли. [6] |
По окончании загрузки быстро нагревают реакционную массу до 325 - 335 и дают кратковременную выдержку при этой температуре. После плавления в реакционной массе содержится около 3 % свободного едкого натра, около 40 % бе-та-нафтолята ( считая на 2-нафтол), около 35 % сульфита натрия и 1 - 2 % непрореагировавшей бета-соли. Выход 2-нафтола в расчете на бета-соль на стадии плавления составляет 94 - 95 % от теоретического. [7]
 |
Схема щелочного плавления бета-соли. [8] |
По окончании загрузки быстро нагревают реакционную массу до 325 - 335 и дают кратковременную выдержку при этой температуре. В - процессе плавления поверхность плава защищают от действия воздуха паровой подушкой. После плавления в реакционной массе, содержится около 3 % свободного едкого натра, около 40 % бе-та-нафтолята ( считая на 2-нафтол), около 35 % сульфита натрия и 1 - 2 % непрореагировавшей бета-соли. Выход 2-нафтола в расчете на бета-соль на стадии плавления составляет 94 - 95 % от теоретического. [9]
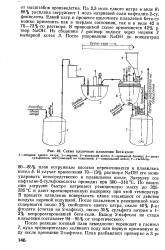 |
Схема щелочного плавлении Бета-соли. [10] |
Загрузку сод нафталин-2 - сульфокислоты проводят при 300 - 310 С. По оконч; нии загрузки быстро нагревают реакционную массу до 325 - 335 С и дают кратковременную выдержку при этой температур В процессе плавления поверхность плава защищают от действи воздуха паровой подушкой. После плавления в реакционной масс содержится около 3 % свободного едкого натра, около 40 % р-нг фтолята ( считая на 2-нафтол), около 35 % сульфита натрия и 1 - 2 % непрореагировавшей бета-соли. Выход 2-нафтола на стади плавления составляет 94 - 95 % от теоретического. [11]
По аналогии можно было ожидать, что сульфогидрат калия будет реагировать с сол ью сульфокислоты сходно с едким кали. Хотя эта реакция изучена не очень обстоятельно, все же видно, что получаемые выходы слишком малы для практического ее использования. По наблюдениям Штадлера [459], при сухой перегонке натриевой соли бензолсульфокислоты с сульфогидратом калия под уменьшенным давлением образуется некоторое количество тиофенола. Натриевая соль 2-нафталинсульфокислоты превращена в смесь 2-нафтола, 2-тионафтола и дисульфида. Выход тионафтола в высшей степени непостоянен без всякой видимой причины. В присутствии сульфида калия выход 2-нафтола повышается. Если сульфо-группа активирована, как, например, в 2 4-динитробензолсульфо-кислоте, реакция с водным раствором сульфогидрата калия идет уже при комнатной температуре [461] с образованием 2 4-динитро-тиофенола. [12]
По аналогии можно было ожидать, что сульфогидрат калия будет реагировать с солью сульфокислоты сходно с едким кали. Хотя эта реакция изучена не очень обстоятельно, gee же видно, что получаемые выходы слишком малы для практического ее использования. По наблюдениям Штадлера [459], при сухой перегонке натриевой соли бензолсульфокислоты с сульфогидратом калия под уменьшенным давлением образуется некоторое количество тиофенола. Ни в этом случае, ни в случае и-бензолди-сульфокислоты основной продукт реакции не идентифицирован. Натриевая соль 2-нафталинеульфокислоты превращена в смесь 2-нафтола, 2-тионафтола и дисульфида. Выход тионафтола в высшей степени непостоянен без всякой видимой причины. В присутствии сульфида калия выход 2-нафтола повышается. Если сульфо-группа активирована, как, например, в 2 4-динитробензолсульфо-кислоте, реакция с водным раствором сульфогидрата калия идет уже при комнатной температуре [461] с образованием 2 4-динитро-тиофенола. [13]
Страницы: 1