Ион - золото
Cтраница 2
Процессы окисления ионов золота Au ( I) в Au ( III) и лимонной кислоты являются нежелательными, и при золочении стремятся свести их к минимуму. Окисление ионов золота приводит к падению катодного выхода по току. Окисление лимонной кислоты сопровождается образованием взвешенных в растворе белых хлопьевидных продуктов окисления, которые, включаясь в катодный осадок, ухудшают его свойства. Из-за несоответствия катодных и анодных выходов по току в ходе эксплуатации электролит подщелачивается. Для поддержания постоянного значения рН добавляют, как правило, лимонную кислоту. По мере накопления лимонной кислоты и продуктов ее окисления раствор густеет, что затрудняет его использование и приводит к сокращению срока службы электролита. [16]
Сильно мешают определению ионы золота, ртути, палладия, галогены, за исключением фтора, и анионы, связывающие серебро. Тяжелые металлы могут быть замаскированы винной кислотой и комплексоном III. К существенным недостаткам метода следует отнести крайнюю светочувствительность комплекса, легкую окисляемость реагента, необходимость очень строгого контроля кислотности и очистки реагента и растворителей. [17]
При открытии Hg2 ион золота осаждают в виде металла сернистой кислотой, олово окисляют до четырехвалентного, сурьму и висмут связывают вик-ной кислотой в комплексные ионы, медь восстанавливают до одновалентной муравьиной кислотой. [18]
При открытии Hg2 ион золота осаждают в виде металла сернистой кислотой, олово окисляют до четырехвалентного, сурьму и висмут связывают винной кислотой в комплексные ионы, медь восстанавливают до одновалентной муравьиной кислотой. [19]
Выполнению реакции мешают ионы золота, меди, серебра, ртути, палладия и платины. [20]
Чувствительной реакцией на ионы золота является восстановление их до металла действием ионов закисной ртути. [21]
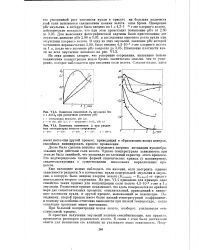 |
Кинетика изменения D0 эмульсий без и с АиС13 при различном значении рВг.| Кинетика изменения Д при различных температурах второго созревания. [22] |
При большой концентрации ионов золота, наоборот, усиливается окислительный процесс. [23]
Контроль полноты извлечения ионов золота смолой осуществлялся взятием проб из каждых 5 л фильтрата, при этом золото в фильтрате не было обнаружено. [24]
Реакция катализируется также ионами золота и ртути. [25]
При открытии Hg2 - ион золота осаждают в виде металла сернистой кислотой, олово окисляют до четырехвалентного, сурьму и висмут связывают винной кислотой в комплексные ионы, медь восстанавливают до одновалентной муравьиной кислотой. [26]
Вследствие положительного стандартного потенциала ионы золота восстанавливаются до металла многими веществами. Для получения покрытий предложено применять глюкозу, формальдегид, гидразин, гипофосфит, борогидрид и др. Лигандом в комплексах золота могут быть амины, хлорид, сульфит, цианид. [27]
Кислоты, ингибированные добавками ионов золота, практически не замедляли коррозию сплава и в большинстве случаев ускоряли коррозию сталей. [28]
При добавках в растворы кислоты ионов золота оказалось, что в H2SO4 коррозия сплава ЭИ461 не тормозится ( образец целиком растворяется), в фосфорной - коррозия сплава замедляется при 0 01 % - ной добавке в 2 5 раза, при 0 1 % - ной добавке значение глубинного показателя остается приблизительно такое же, как и без добавки. Стойкость стали Х23Н28МЗДЗТ и в серной и в фосфорной ингибированных кислотах понижается. Коррозия стали 1Х18Н9Т замедляется при 0 1 % - ной добавке золота в H SO4 всего лишь в 2 1 раза, а в фосфорной кислоте при такой же добавке коррозия ее, наоборот, повышается. [29]
В настоящее время на десятках заводов ионы золота из отработанных растворов и промывных вод улавливаются на анионообменном волокне. [30]
Страницы: 1 2 3 4