Выход - окисление
Cтраница 2
Наклон ее к оси абсцисс в первые минуты соответствует выходу окисления ионов Fe2, равному 63 экв. [16]
Здесь АС - изменение концентрации органического вещества в процессе радиационного окисления, мг / л; М - молекулярный вес; G - радиационно-химичесшш выход окисления, молекул / 100 эв; Д - доза, Мрад; 0 95 - коэффициент размерности. [17]
 |
Зависимость выхода окисления двухвалентного железа от его концентрации, по данным Дейнтона и Саттона. [18] |
Несколько позже Пикаев и Глазунов [7], исследуя влияние концентрации и мощности дозы ( при значительно более высоких значениях последней, чем в работе [5]) на выход окисления ионов двухвалентного железа в такой системе, использовали для описания экспериментальных данных в точности тот же механизм. [19]
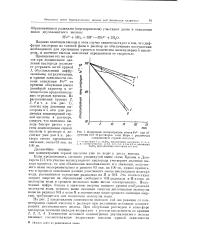 |
Изменение концентрации ионов Fes при облучении 0 01 М растворов соли Мора с различным содержанием сорной кислоты. [20] |
Падение величины выхода в этом случае свидетельствует о том, что диффузия кислорода из газовой фазы в раствор не обеспечивает поступления необходимого для протекания процесса количества молекулярного кислорода, и значение выхода окисления определяется ее скоростью. [21]
Несколько позднее Фрикке и Харт 12 ] обнаружили, при облучении рентгеновскими лучами растворов нитрита, протекание радиационно-химического процесса образования нитрата, с одновременным выделением эквивалентного количества молекулярного водорода. По данным этих авторов, выход окисления нитрита не зависит от его исходной концентрации в растворе ( в изученных пределах от 5 - 10 - 5 до 1СГ1 М), от значения рН раствора в пределах от 2 до 11 и составляет 0 55 jiM / кг. [22]
Показано, что кислород, находящийся в растворе красителя, при облучении на воздухе играет роль защитного вещества, связывающего восстановительную часть продуктов радиолиза воды. Образующиеся при этом радикалы Н02 реагируют с частью свободных гидроксилов, из-за чего снижается выход окисления красителя. [23]
Действительно, при радиационном окислении м-гептана, к-нонана, изооктана повышение мощности дозы приводит к уменьшению выходов окисления и к смещению температур перехода ТП1 и Т 2 в область более высоких температур. [24]
Нитрат натрия также снижает выход окисления Pu ( IV), но не так сильно, как азотная кислота. Следовательно, чем больше кислотность раствора при одной и той же концентрации ионов NO -, тем меньше выход окисления. [25]
Теоретическое рассмотрение процесса радиолиза водных растворов под действием жестких - у-лучей и быстрых электронов [2, 3] объясняет равномерное распределение активных частиц, а следовательно и / - закономерности, в широком интервале значений мощности дозы и концентрации акцепторов. Существование / - закономерностей показано для кислых растворов трехвалентного титана и двухвалентного железа [4, 5], где сдвиги кривых выхода окисления Ti ( III) и Fe ( II) точно соответствуют величине / 2 log ( Ii / fz), ожидаемой на основании теории / - закономерностей. Экспериментально показано, что при радиолизе кислого водного раствора Н2О2, насыщенного водородом, также наблюдается точное выполнение / - закономерностей. [26]
Окислительные свойства атомарного водорода по отношению к иону двухвалентного железа, впервые постулированные Вейссом, первоначально отвергались рядом исследователей. Чтобы проверить, способен ли атомарный водород к окислению иона Fe2, мы исследовали влияние концентрации молекулярного водорода на выход окисления Fe21 в растворах, насыщенных водородом под давлением. [27]
Для 10 - 2 М раствора фенола при мощности дозы 200 рад / сек выход убыли фенола составляет 5 молекул / 100 эв, а при мощности дозы. Весьма вероятно, что окисление более сложных фенолов, придающих запах воде, тоже будет протекать по цепному механизму. Если бы уменьшение мощности дозы повысило в таком случае выход окисления, это дало бы возможность значительно снизить дозу, необходимую для дезодорации, и тем самым удешевить процесс. [28]
Реакция окисления раствора соли Мора под действием излучений с давних пор применяется в качестве дозиметрической. До настоящего времени она остается одной из лучших реакций этого типа по чувствительности, надежности и воспроизводимости результатов проводимых с ее помощью измерений. Изучение этой реакции началось особенно интенсивно с развитием новой области физической химии - радиационной химии. Всеобщий интерес исследователей, работающих в этой отрасли химии, к реакции окисления Fe2 объясняется не только стремлением использовать ее чисто практически в дозиметрии, но, главным образом, желанием всесторонне изучить посредством этой вторичной радиационно-химическои реакции механизм процессов, протекающих в водном растворе под действием ионизирующих излучений. Этими исследователями изучены основные свойства реакции, в частности, установлена прямолинейная зависимость концентрации образующегося Fe3 от дозы, а также независимость выхода окисления от изменения концентрации двухвалентного железа в пределах от 5 - 10 - 5 и до. [29]
Страницы: 1 2