Выход - цинк
Cтраница 3
В; g - электрохимический эквивалент цинка, г / ( А - ч); Вт - выход цинка по току, доли единицы. [31]
 |
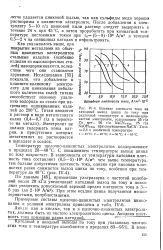
Зависимость потенциала цинкового катода от добавки желатины. [32] |
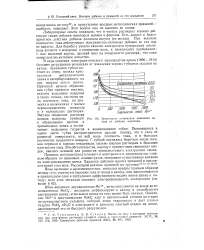
Ионы марганца: двухвалентные Мп2, легко окисляются на аноде до семивалентных МпО; последние диффундируют к катоду и способствуют растворению цинка; этим выход цинка по току может быть снижен. Окисление Мп2 и восстановление МпО - идет в значительной степени до стадии четырехвалентного сульфата, который легко гидролизует и дает хлопья гидрата МпО2 - пН О в электролите и довольно плотный осадок на аноде, защищающий его от быстрого разрушения. [33]
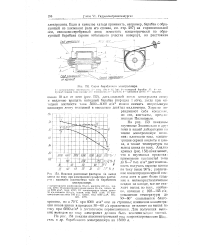 |
Схема барабанного электролизера. [34] |
На рис. 153 показаны изученные Знаменским и другими в нашей лаборатории на таком электролизере влияния: плотности тока, концентрации серной кислоты и цинка, а также температуры на выход цинка по току. Анализ кривых ( рис. 153) показывает, что в изученных пределах: применение плотностей тока до 6 - 7 тыс. а / мг дает возможность получать выходы цинка по току выше 90 %; увеличение концентрации серной кислоты хотя и дает более гладкие и. [35]
По средним значениям ф и фр рассчитывают с помощью кинетического уравнения ( см. выше) среднюю парциальную силу тока, с которой происходило выделение водорода в каждом электролизере и вычисляют выход цинка по току. [36]
Сколько цинка можно получить из: а) 0 5 т; б) 250 кг; в) 126 кг галмея при условии, что руда содержит 94 % углекислого цинка, а выход цинка составляет 98 % от теоретически возможного. [37]
Вследствие того, что нормальный потенциал цинка равен - 0 76 в, при электролитическом осаждении цинка из водных растворов его солей на катоде в первую очередь и преимущественно должен совершаться электрохимический процесс разряда ионов водорода, и выход цинка по току должен быть близок к нулю. Однако, цинк обладает той особенностью, что водород на нем имеет большое перенапряжение и почти не выделяется на катоде при обычных условиях элек - тролиза. Благодаря высокому перенапряжению водорода на цинке, становится возможным осаждение цинка из водных растворов. Любые условия, снижающие перенапряжение водорода на цинке, вызывают резкое снижение выхода по току цинка с одновременным изменением качества покрытий. [38]
Какая масса цинковой руды, содержащей ZnS 4 5 %, должна перерабатываться для годовой выработки цинка массой 10000 т, если в результате флотации руды получают концентрат с массовой долей цинка 0 4С при степени извлечения 85 %, а выход цинка в процесса переработки концентрата в оксид цинка, восстановления его и перегонки металла составляет 92 % от теоретического. [39]
Таким образом, кислотность электролита при электролизе увеличивается. Выход цинка по току зависит от распределения количества электричества между двумя реакциями электролиза. [40]
Кроме того, в начале опыта и через каждые 30 мин измеряют напряжение на электролизерах. Затем определяют выход цинка по току весовым методом. По полученным данным находят удельный расход энергии. [41]
По закону Фарадея при пропускании 26 8 А ч электричества ( IF) на электродах испытывает превращение один грамм-эквивалент вещества. Так как выход цинка на катоде составляет 50 %, то на нем выделится 0 5 г-экв цинка, и количество цинка в электролите уменьшится также на 0 5 г-экв. Если анод графитовый, то цинк в раствор не поступает и в процессе электролиза количество цинка в растворе уменьшится на 0 5 г-экв. Если анод цинковый, то при прохождении через него 26 8 А ч электричества ( IF) при 100 % - ном выходе по току растворяется 1 г-экв цинка. Так как в раствор переходит 1 г-экв, а осаждается на катоде 0 5 г-экв цинка, то суммарное увеличение количества цинка в растворе равно 0 5 г-экв. [42]
По закону Фарадея при пропускании 26 8 А - ч электричества ( IF) на электродах испытывает превращение 1 моль эквивалентов вещества. Так как выход цинка на катоде составляет 50 %, то на нем выделится 0 5 моль эквивалентов цинка и количество цинка в электролите уменьшится также на 0 5 моль эквивалентов. Если анод графитовый, то цинк в раствор не поступает и в процессе электролиза количество цинка в растворе уменьшится на 0 5 моль эквивалентов. Если анод цинковый, то при прохождении через него 26 8 А - ч электричества ( IF) при 100 % - ном выходе по току растворяется 1 моль эквивалентов цинка. Так как в раствор переходит 1 моль эквивалентов, а осаждается на катоде 0 5 моль эквивалентов цинка, то суммарное увеличение количества цинка в растворе равно 0 5 моль эквивалентов. [43]
Температуру щелочно-цианистых электролитов поддерживают в пределах 20 - 40 С. С повышением температуры выход цинка по току возрастает. [45]
Страницы: 1 2 3 4 5