Выход - галлий
Cтраница 1
Выход галлия составляет 0 4 г с каждого квадратного дециметра поверхности катода в сутки. [1]
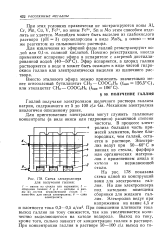 |
Схема электролизера для получения галлия. [2] |
При повышении плотности тока выход галлия по току снижается, так как увеличивается количество выделяющегося на катоде водорода. Выход по току, кроме того, сильно зависит от концентрации галлия в растворе. [3]
Увеличение катодной плотности тока приводит к некоторому уменьшению выхода по току, однако увеличивается выход галлия на единицу площади катода. После этого электролит возвращают на растворение концентрата. Осажденный галлий стекает на дно ванны. Так как поверхность жидкого галлия мала, обратное растворение металла в электролите незначительно. Часть галлия, обогащенная примесями, в частности железом, может образовать пасту, прилипающую к катоду; оттуда ее приходится периодически соскребать. [4]
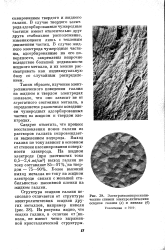 |
Электронномикроскопи-ческие снимки электролитических осадков галлия ( а и никеля ( б. [5] |
Следует отметить, что процесс восстановления ионов галлия из растворов галлата сопровождается выделением водорода. Выход галлия по току зависит в основном от степени пассивирования поверхности электрода. Более высокий выход металла по току на жидком электроде связан с меньшей стабильностью пассивной пленки на жидком галлии. [6]
Электроды ранее изготовлялись из платины, в настоящее время - из нержавеющей стали или никеля. С повышением температуры выход галлия по току и скорость его выделения увеличиваются за счет увеличения подвижности его ионов. [7]
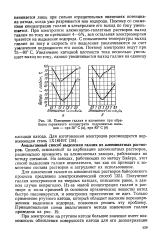 |
Поведение галлия и алюминия при обработке первичного концентрата гидроокисью кальция - при 50 С ( а, при 85 С ( 6. [8] |
Поэтому со снижением концентрации галлия в электролите его выход по току уменьшается. При электролизе алюминатно-галлатных растворов выход галлия по току не превышает 4 - 6 %, вся остальная электроэнергия тратится на выделение водорода. С повышением температуры выход галлия по току и скорость его выделения увеличиваются за счет увеличения подвижности его ионов. Поэтому электролиз ведут при 75 - 80 С. [9]
Извлечение галлия из раствора может быть проведено цементацией амальгамой натрия из 1 - 8 N раствора NaOH [328.] Ускорение извлечения достигается увеличением концентрации амальгамы ( 0 25 - 1 5 %) и скорости перемешивания ( 350 - 1400 об / мин) при 20 - 80 С. В 4 5 и 8 5 N растворах NaOH удается оолностью отделить галлий от алюминия и хрома; в присутствии 5 мг V выход галлия в амальгаму уменьшается, а при содержании 20 мг V цементация галлия совсем не происходит. [10]
При электролизе на ртутном катоде большое значение имеет обновление за счет перемешивания поверхности катода для его деполяризации и ускорения диффузии галлия в ртуть. Выход галлия по току остается небольшим - порядка нескольких процентов; в основном ток расходуется на выделение водорода и натрия, а также на восстановление примесей. В результате получается натриево-галлиевая амальгама, которая далее разлагается. Недостаток процесса - большой расход ртути, которая распыляется и переходит в алюминатный раствор. [11]
При электролизе на ртутном катоде большое значение имеет обновление за счет перемешивания поверхности катода для его деполяризации и ускорения диффузии галлия в ртуть. Выход галлия по току остается небольшим - порядка нескольких процентов; в основном ток расходуется на выделение водорода и натрия, а также на восстановление примесей. В результате получается натриево-галлиевая амальгама, которая далее разлагается. Недостаток процесса - большой расход ртути, которая распыляется и переходит в алюминатный раствор. [12]
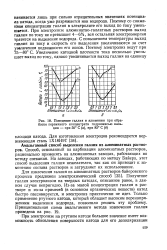 |
Поведение галлия и алюминия при обработке первичного концентрата гидроокисью кальция - при 50 С ( а, при 85 С ( 6. [13] |
Поэтому со снижением концентрации галлия в электролите его выход по току уменьшается. При электролизе алюминатно-галлатных растворов выход галлия по току не превышает 4 - 6 %, вся остальная электроэнергия тратится на выделение водорода. С повышением температуры выход галлия по току и скорость его выделения увеличиваются за счет увеличения подвижности его ионов. Поэтому электролиз ведут при 75 - 80 С. [14]
Страницы: 1