Ион - осаждающийся металл
Cтраница 1
Ионы осаждающегося металла переводят в состав комплексных солей. [1]
Концентрация ионов осаждающегося металла сказывается на величине образующихся кристаллов. [2]
Все факторы, обусловливающие разряд ионов осаждающегося металла при значении потенциала, близком к равновесному, способствуют преимущественному росту кристаллов, имеющихся на катодной поверхности, и приводят к образованию крупнокристаллических осадков. Если же разряд ионов сопровождается значительной катодной поляризацией, то происходит преимущественное образование новых зародышей, и осадки получаются мелкокристаллическими. [3]
При получении контактных покрытий в гальванотехнике, где концентрация ионов осаждающегося металла постоянна в течение всего процесса, определение порядка реакции контактного обмена не представляет особого интереса. [4]
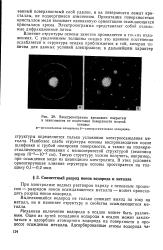 |
Электронограмма хромового покрытия в зависимости от подготовки поверхности медной. [5] |
При электролизе водных растворов наряду с основным процессом - разрядом ионов осаждающегося металла - может происходить разряд ионов водорода. [6]
 |
Схема нанесения гальванических покрытий. [7] |
При гальваническом методе нанесения металлических покрытий покрываемые изделия помещают в электролит, содержащий ионы осаждающегося металла, и соединяют с отрицательным полюсом источника постоянного тока. Покрываемое изделие, таким образом, является катодом. [8]
Катодная поляризационная кривая снимается в исследуемом растворе, а анодная - в том же растворе, но не содержащем ионов осаждающегося металла. [9]
Исходя из этих основных положений, можно рассчитывать на получение катодных осадков с одинаковой кристаллической структурой, независимо от того, происходило ли осаждение при низкой плотности тока из разбавленного электролита, или при высокой плотности тока из концентрированного электролита или при очень высокой плотности тока из концентрированного электролита, подвергаемого подогреву и интенсивному перемешиванию. Решающую роль играет величина потенциала, при котором происходит разряд ионов осаждающегося металла. [10]
Сопряженные реакции восстановления ионов металла и окисления восстановителя могут протекать достаточно эффективно только на поверхности, обладающей каталитическими свойствами, поэтому обрабатываемый материал подвергают еще одной специальной обработке, называемой активацией. Сущность процесса активации состоит в придании поверхности материала каталитических свойств по отношению к реакции восстановления ионов осаждающегося металла. [11]
Поверхностно активные вещества ( в количестве 10 г / л) в той или иной мере оказывают влияние на катодный процесс, улучшают структуру, наружный вид покрытия, а иногда повышают рассеивающую способность электролита. Влияние таких веществ на электродные прощессы объясняют возникновением в электролите адсорбционных соединений комплексного строения, состоящих из ионов осаждающегося металла и поверхностно активного вещества. Создаются затруднения для образования ионов металла в приэлектродном слое электролита. Если эти добавки образуют комплексные соединения с анионами электролита, то они должны оказывать влияние как на катодный, так и на анодный процессы. [12]
Так, например, в работе Плаксина и Суворовской [91], данные которых описываются формулой ( 25), указывается на катодный диффузионный контроль, а не актив ациооныи, в предположении которого эта формула была выведена. Доказывая спра ведливость уравнения ( 25), Берман ссылается на его согласие с формулой Кудры и Гитман [107], связывающей концентрацию ионов осаждающегося металла и промежуток времени, проходящий до возникновения рыхлых осадков. Следует, однако, иметь в виду, что рыхлые осадки образуются чаще при наличии заметных диффузионных ограничений катодного процесса. Прямолинейная зависимость h - У Т свидетельствует iCKOipee о диффузионном, а не об яктяеащюнгаом контроле скорости цементации. [13]
Нанесение гальванических покрытий основано на кристаллизации металлов из водных растворов их солей при прохождении постоянного тока. Гальванотехническая система представляет собой электролитическую цепь, состоящую в простейшем случае из двух электродов - катода и анода - и электролита, содержащего ионы осаждающихся металлов. [14]
Известно, что из растворов комплексных солей, например цианистых солей меди, цинка, кадмия, серебра и др., получаются осадки с более тонкой структурой, чем из соответствующих растворов простых солей. Однако имеется достаточно оснований утверждать, что решающее влияние на структуру оказывает не специфическая особенность аниона ( конечно, нельзя утверждать, что анион не играет никакой роли), а активность ионов осаждающегося металла и связанная с ней величина катодной поляризации. Принципиально можно получить катодные-осадки с одинаковой кристаллической структурой как из растворов комплексных, так и простых солей, если величина катодной поляризации в обоих случаях одинакова. [15]
Страницы: 1 2