Ион - платиновый металл
Cтраница 1
Ионы платиновых металлов проявляют большую склонность к комплексообразованию. Для Pd ( II) и Pt ( II) типичны соединения с координационным числом 4, например, K. Pt ( NH3) 4 ] Ci2, В большинстве случаев платиновые металлы образуют комплексные соединения с координационным числом 6, Ниже приводятся примеры образования некоторых комплексных соединений. [1]
Ионы платиновых металлов проявляют большую склонность к комплексообразованию. Для Pd ( II) ц Pt ( II) типичны соединения с координационным числом. Ниже приводятся примеры образования некоторых комплексных соединений. [2]
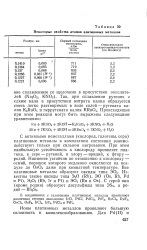 |
Некоторые свойства атомов платиновых металлов. [3] |
Ионы платиновых металлов проявляют большую склонность к комплексообразованию. [4]
Ионы платиновых металлов проявляют большую склонность к комплексообразованию. Ниже приведены примеры образования некоторых комплексных соединений. [5]
Ионы платиновых металлов проявляют большую склонность к комплексообразованию. [6]
Большую часть соединений гексацидового типа образуют трех - и четырехвалентные катионы, главным образом Со3, Cr3, Fe3 и ионы платиновых металлов соответствующей валентности. Со ( CN) 6 ] 3 -, [ Со ( OH) 3 ( NO2) 3 ] 3, [ Со ( С2О4) 3 ] 3, из соединений хрома - [ Сг ( CN) e ] 3, [ Cr ( SCN) 6 ] 3, [ Сг ( С2О4) зР, из соединений железа - [ Ре ( CN) e ] 3, [ FeF6 ] 3, [ Fe ( PO4) 2 ] 3 - Для ионов платиновых металлов характерны соединения как гексацианового, так и гексагалогенового типа. [7]
 |
Физико-химические свойства оксидов рутения и осмия. [8] |
Как правило, все соединения платиновых металлов обладают характерной окраской, резко выраженными окислительными свойствами и относительно невысокой устойчивостью по отношению к нагреванию. Ионы платиновых металлов легко образуют комплексные соединения. [9]
Возможность практического проведения той или иной окислительно-восстановительной реакции определяется рядом факторов и по этой причине обычно устанавливается экспериментальным путем. Например, экспериментально найденная последовательность восстановления ионов платиновых металлов в растворе их комплексных хлоридов до элементарного состояния не соответствует значениям нормальных окислительно-восстановительных потенциалов систем [ МеС1б ] 3 / Меили [ МеС14 ] 2 - / Ме. Она отвечает следующему ряду: PdPtRhIr, который совпадает с рядом констант нестойкости комплексных хлоридов этих элементов. На последовательности восстановления металлов, отвечающей этому ряду, основано групповое отделение золота, палладия и платины от родия и иридия. [10]
Возможность практического проведения той или иной окислительно-восстановительной реакции определяется рядом факторов и по этой причине обычно устанавливается экспериментальным путем. Например, экспериментально найденная последовательность восстановления ионов платиновых металлов в растворе их комплексных хлоридов до элементарного состояния не соответствует значениям нормальных окислительно-восстановительных потенциалов систем [ МеС16 ] 3 - / Ме или [ МеСЦ ] 2 - / Ме. Она отвечает следующему ряду: PdPtRhIr, который совпадает с рядом констант нестойкости комплексных хлоридов этих элементов. На последовательности восстановления металлов, отвечающей этому ряду, основано групповое отделение золота, палладия и платины от родия и иридия. [11]
Большую часть соединений гексацидового типа образуют трех - и четырехвалентные катионы, главным образом Со3, Cr3, Fe3 и ионы платиновых металлов соответствующей валентности. Со ( CN) 6 ] 3 -, [ Со ( OH) 3 ( NO2) 3 ] 3, [ Со ( С2О4) 3 ] 3, из соединений хрома - [ Сг ( CN) e ] 3, [ Cr ( SCN) 6 ] 3, [ Сг ( С2О4) зР, из соединений железа - [ Ре ( CN) e ] 3, [ FeF6 ] 3, [ Fe ( PO4) 2 ] 3 - Для ионов платиновых металлов характерны соединения как гексацианового, так и гексагалогенового типа. [12]
Страницы: 1