Максимальный выход - комплекс
Cтраница 1
Максимальный выход комплексов наблюдается при рН 2 2, а константы устойчивости равны 3 6 - 106 и 4 8 - 107 соответственно. [1]
Постоянное значение рН выбирают оптимальным, обеспечивающим максимальный выход комплекса, на основании предварительных опытов, или теоретических соображений. [2]
Это постоянное значение рН выбирают оптимальным, обеспечивающим максимальный выход комплекса, на основании предварительных опытов или теоретических соображений. [3]
Решение уравнения (1.18) позволяет найти оптимальное значение рН раствора, при котором обеспечивается максимальный выход комплекса с протонированной формой HmRm-7 реагента. [4]
Решение уравнения (1.18) позволяет найти оптимальное значение рН раствора, при котором обеспечивается максимальный выход комплекса с протонированной формой HmRm - реагента. [5]
Решение уравнения (5.30) v позволяет найти оптимальное значение рН раствора, при котором обеспечивается максимальный выход комплекса с протонированной формой H R - 1 фотометрического реагента. [6]
Более сложно решается вопрос о выборе значения рН раствора для проведения фотометрического определения в тех случаях, когда при рН максимального выхода комплекса значительная часть фотометрического реагента находится в такой форме, спектр поглощения которой очеиь близок к спектру поглощения анализируемого соединения. В этих случаях проведение анализа при рН раствора, обеспечивающем максимальный выход светопоглощающего соединения, из-за значительного поглощения самого реагента сопряжено с большими ошибками, особенно при определении малых количеств анализируемого элемента. В этих условиях фотометрирование растворов целесообразно проводить при меньших значениях. [7]
Щри проведении процесса с водным раствором карбамида основным фактором является концентрация карбамида. Насыщенному раствору карбамида соответствует максимальное извлечение к-парафинов и, следовательно, максимальный выход комплекса; при уменьшении концентрации карбамида выход комплекса снижается. В связи с этим непременным условием при осуществлении данного варианта процесса является поддержание насыщенности раствора на всем этапе комплексообразованияс Сохранение насыщенности раствора обеспечивается, во-первда, применением растворов, насыщенных при температурах, более высоких, чем температура комплексообразования, а, во-вторых, постепенным снижением температуры реакционной смеси. [8]
 |
Спектр поглощения моносульфосалицилата железа. [9] |
Однако выход комплексов а зависит от рН раствора. Как видно из рис. 1.26, реакцию следует проводить при значениях рН, соответствующих максимальному выходу комплекса. [10]
 |
Графическое определение оптимального интервала рН в фотометрическом анализе ( комплексы MR2 или MRR, [ CR ] [ CR j Ы0 -. моль / л. [11] |
В этих случаях проведение анализа при рН раствора, обеспечивающем максимальный выход светопоглощающего соединения, из-за большого поглощения самого реагента сопряжено со значительными погрешностями, особенно при определении малых количеств анализируемого элемента. В этих условиях фотометрирование растворов целесообразнее проводить при меньших значениях рН раствора, при которых хотя и не достигается максимальный выход комплекса, но содержание светопоглощающей формы реагента также не превышает 10 - 15 % от светопоглощения анализируемого комплекса. [12]
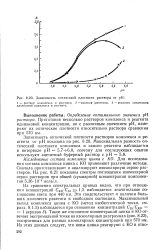 |
Зависимость оптической плотности раствора от рН. [13] |
Из сравнения спектральных кривых видно, что при отношении концентраций Cno / CZa 1 5 наблюдается значительное поглощение света при 440 нм. Это свидетельствует о наличии больших количеств реагента в свободном состоянии. Максимальный выход комплекса цинка с КО ( метод изобестической точки, см. разд. Такое же отношение концентраций цинка и КО отвечает экстремальной точке на изомолярных диаграммах ( рис. 8.22), построенных для разных изомолярных концентраций при 570 нм. [14]
Более сложно решается вопрос о выборе значения рН раствора для проведения фотометрического определения в тех случаях, когда при оптимальном значении рН значительная часть фотометрического реагента находится в реакционной форме, спектр поглощения которой очень близок к спектру анализируемого соединения. В этих случаях проведение анализа при рН раствора, обеспечивающем максимальный выход светопоглощающего соединения, из-за большого поглощения самого реагента сопряжено со значительными погрешностями, особенно при определении малых количеств анализируемого элемента. В этих условиях фотометрирование растворов целесообразнее проводить при меньших значениях рН раствора, при которых хотя и не достигается максимальный выход комплекса, но содержание светопоглощающей формы реагента также не превышает 10 - 15 % от светопоглощения анализируемого комплекса. [15]
Страницы: 1