Действительный выход - продукт
Cтраница 1
Действительный выход продукта х в эндотермических процессах изменяется подобно равновесному. [1]
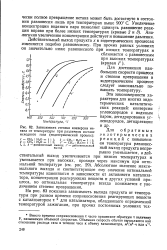 |
Зависимость степени конверсии ме-тана от температуры при различном составе исходного газа ( эндотермический процесс. [2] |
Аналогично увеличению концентрации действует и повышение давления. Действительный выход продукта х в эндотермических процессах изменяется подобно равновесному. [3]
СО, растет с повышением температуры. При стехиометрическом расходе водяного пара ( кривая /) практически полное превращение метана может быть достигнуто в состоянии равновесия лишь при температурах выше 900 С. Действительный выход продукта х в эндотермических процессах изменяется подобно равновесному. [4]
Приведенные примеры показывают, насколько важно научиться владеть химическими расчетами. Без них немыслимы ни правильно организованная работа производства, ни его контроль. Величина действительного выхода продукта определяется в основном характером самого химического процесса и применяемым для его проведения технологическим методом, но частр дает также возможность судить и о качестве работы. [5]
Приведенные примеры показывают, насколько важно научиться владеть химическими расчетами. Без них немыслимы ни правильно организованная работа производства, ни его контроль. Значение действительного выхода продукта определяется в основном характером самого химического процесса и применяемым для его проведения технологическим методом, но часто дает также возможность судить и о качестве работы. [6]
Приведенные примеры показывают, насколько важно научиться владеть химическими расчетами. Без них немыслимы ни правильно организованная работа производства, ни его контроль. Величина действительного выхода продукта определяется в основном характером самого химического процесса и применяемым для его проведения технологическим методом, но дает также возможность судить и о качестве работы. [7]
Экзотермические обратимые реакции интенсифицируются при повышении температуры только за счет увеличения константы скорости прямой реакции. Происходит это вследствие того, что скорость обратной эндотермической реакции с повышением температуры возрастает, начиная с некоторого предела быстрее, чем прямой. В результате действительный выход продукта х повышается с ростом температуры лишь до некоторого предела ( максимума), соответствующего оптимальной температуре. При повышении температуры сверх оптимальной и действительный, и равновесный выходы падают. [8]
При наличии катализатора определенного состава и структуры наибольшее практическое значение имеет температурный режим каталитических процессов. Для процессов, идущих в кинетической области, повышение температуры всегда увеличивает скорость приближения процесса к состоянию равновесия. В результате этого закономерности изменения суммарной скорости реакции ( действительного выхода продукта х) для экзотермических и эндотермических реакций совершенно различны. [9]
При наличии катализатора определенной активности наибольшее практическое значение имеет температурный режим каталитических процессов. Для процессов, идущих в кинетической области, повышение температуры всегда увеличивает скорость приближения процесса к состоянию равновесия, но равновесный выход хр с повышением температуры увеличивается для эндотермических и уменьшается для экзотермических процессов. В результате этого закономерности изменения суммарной скорости реакции ( действительного выхода продукта х) для экзотермических и эндетермических реакций совершенно различны. [10]
При наличии катализатора определенной активности наибольшее практическое значение имеет температурный режим каталитических процессов. Для процессов; идущих в кинетической области, повышение температуры всегда увеличивает скорость приближения процесса к состоянию равновесия, но равновесный выход хр с повышением температуры увеличивается для эндотермических и уменьшается для экзотермических процессов. В результате этого закономерности изменения суммарной скорости реакции ( действительного выхода продукта хф) для экзотермических и эндотермических реакций совершенно различны. [11]
Страницы: 1