Ион - нитрит
Cтраница 1
Ионы нитрита ( NOa -) довольно широко распространены в поверхностных и грунтовых водах, но обычно в очень небольшом количестве. Повышенное количество азотистой кислоты в подземной воде может появляться в процессе окисления аммиачных соединений и разложения органических веществ, а также при восстановлении нитратов в нитриты. Окисление аммиачных соединений нередко вызывается деятельностью нитрифицирующих бактерий. Некоторые виды бактерий, обитающие в загрязненных водах ( например, кишечная палочка), проникают в подземные воды с нечистотами. [1]
Ион нитрита, являющийся важным лигандом, изучен довольно тщательно. [2]
Ионы нитрита в кислотном растворе реагируют с первичными ароматическими аминами с образованием солей диазония, которые затем взаимодействуют с каким-либо ароматическим соединением, содержащим аминные или гидроксильные группы, с образованием азосоединения, удобного для визуального или фотометрического определения. Реакция очень селективна и чувствительна и дает возможность идентифицировть 1 мкг нитритного азота в 1 л раствора. [3]
В ионе нитрита этим центром является атом азота, поэтому преимущественно образуется нитроалкан. Если же преобладает 8к1 - характер, то образуется главным образом алкилнитрит. [4]
В этом ряду ион нитрита согнут почти до тетрагонального угла; двуокись азота, которая является стабильным свободным радикалом, имеет слегка согнутую конфигурацию, и ион нитрония линеен. [5]
Образующийся при этом ион нитрита определяют колориметрически с реактивом Грисса-Илосвая. [6]
Чувствительность определения 1 мкг иона нитрита в определяемом объеме раствора, что соответствует 2 8 мкг нитроциклогексана. [7]
Инфракрасный спектр и силовые постоянные иона нитрита. [8]
Таким образом, на восстановление шести ионов нитрита, входящих в состав осадка, затрачивается 36 г-экв железа, а на восстановление трехвалентного кобальта - еще 1 г-экв. [9]
Облучение растворов нитрита калия вызывает окисление ионов нитрита в нитрат-ионы свободными гидроксилами, образующимися при радиолизе воды. Скорость процесса пропорциональна концентрации нитрита в растворе. В щелочных растворах она незначительна, а в кислых - достаточно велика. Этим обусловлено падение выхода восстановления нитрата в нитрит при облучении кислых растворов. [10]
К препарату ( около 0 001 г иона нитрита) прибавляют 2 капли раствора дифениламина; появляется синее окрашивание. [11]
Можно также предположить, что при алкилировании иона нитрита: 6N - б: алкильный остаток частично присоединяется к неподеленной электронной паре азота, а частично - к такой же паре кислородного атома; в первом случае образуется нитросоединение, во втором - эфир азотистой кислоты. [12]
Можно также предположить, что при алкилировании иона нитрита: O - - - - N-О: алкильный остаток частично присоединяется к неподеленной электронной паре азота, а частично - к такой же паре кислородного атома; в первом случае образуется нитросоединение, во втором - эфир азотистой кислоты. [13]
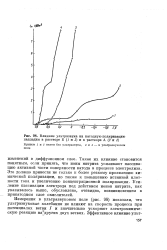 |
Влияние ультразвука на катодную поляризацию палладия в растворе Б ( 1 и 3 и в растворе А ( 2 и 4. [14] |
Такое их влияние становится понятным, если принять, что ионы нитрита усиливают пассивацию активной части поверхности катода в процессе электролиза. Это должно привести не только к более резкому проявлению химической поляризации, но также к повышению истинной плотности тока и увеличению концентрационной поляризации. Усиление пассивации электрода под действием ионов нитрита, как указывалось выше, обусловлено, очевидно, возникновением в прикатодном слое окислителей. [15]
Страницы: 1 2 3 4