Ион - бериллий
Cтраница 1
 |
Растворимость гидроокиси бериллия Ве ( ОН2 и формы существования бериллия в растворах в за-ь, L висимости от рН. [1] |
Ионы бериллия обнаруживают очень большое сходство с ионами алюминия, давая много одинаковых реакций. [2]
Ионы бериллия имеют меньшие размеры, чем ионы магния. Однако образование нитрида магния начинается при температуре 560вС, а нитрида бериллия лишь при 900 С. [3]
Ионы бериллия не обнаружены ни в кристаллах его соединений, ни в растворах и расплавах последних. [4]
Ион бериллия ( II) имеет меньшие размеры и дает более прочные комплексы, чем остальные щелочноземельные металлы. Координируется он преимущественно с четырьмя лигандами. Комплексы бериллия ( II) обладают почти, правильной тетраэдрической структурой. [5]
Ион бериллия обладает меньшим радиусом, чем ионы других элементов II группы и создает поле большей напряженности. Поэтому Be ( ОН) г и ВеО обладают амфотерными свойствами. Однако как кислые, так и основные свойства гидроксида бериллия выражены слабо. [6]
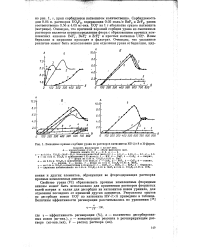 |
Выходные кривые сорбции урана из растворов катионитом КУ-2Х8 в Н - форме. [7] |
Ионы бериллия и циркония проходят в фильтрат. [8]
Ионы бериллия, магния, кальция, стронция и цинка не осаждаются и не экстрагируются в виде дитиофосфатов. [9]
Тримерные ионы бериллия тоже могут присутствовать в растворах в небольших количествах. [10]
Гримерные ионы бериллия тоже могут присутствовать в растворах в небольших количествах. [11]
Все ионы бериллия бесцветны. [12]
Все ионы бериллия бесцветны. [13]
Для иона бериллия плотность заряда и теплота образования твердых аммиакатов и гидратов особенно велики. [14]
Отделение ионов бериллия от алюминия посредством ( МН4) оСОз не является полным. Рекомендуется кипячение гидроокисей алюминия и бериллия в 1 М растворе ( МЬЦШСОз. При этих условиях А1 ( ОН) з остается в осадке, а комплексная соль бериллия количественно переходит в раствор. [15]
Страницы: 1 2 3 4