Ион - палладий
Cтраница 1
Ионы палладия, реагируя с двухвалентным оловом, также дают на бумаге окрашенное пятно, препятствуя открытию платины, однако в присутствии диметилглиоксима окрашивание обусловливается только платиной. Поэтому для открытия платины в присутствии палладия бумажку смачивают раствором диметилглиоксима, наносят каплю испытуемого раствора, снова смачивают раствором диметилглиоксима, затем раствором хлорида олова ( II) и раствором иодида калия. [1]
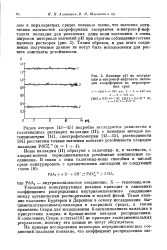 |
Влияние рН на экстракцию ое-нитрозо-р-нафтолата палладия хлороформом из перхлоратных сред. [2] |
Ионы палладия ( II) образуют с галогенид - и, в частности, с хлорид-ионами термодинамически устойчивые комплексные соединения. [3]
Ионы палладия и платины можно иногда рассматривать как окислители. Из растворов PtCh при действии восстановителей выделяется платина. Ионы благородных металлов характеризуются исключительно выраженной способностью к комплексообразованию. Из большого числа комплексных соединений платины в лабораторной практике находит применение платинохлористоводородная кислота, применяемая как реактив на ион калия. [4]
Ионы палладия и платины, как ионы благородных металлов, обладают сильными окислительными свойствами. Из растворов Р1СЦ при действии избытка восстановителей выделяется платина. Ионы благородных металлов характеризуются исключительно выраженной способностью к комплексообразованию. [5]
Ионы палладия и платины, как ионы благородных металлов, обладают сильными окислительными свойствами. Из растворов Р1С14 при действии избытка восстановителей выделяется платина. Ионы благородных металлов характеризуются исключительно выраженной способностью к комплексо-образованию. Из большого числа комплексных соединений платины в лабораторной практике находит применение, как реактив на ион калия, платинохлористоводородная кислота. [6]
Ионы палладия и платины, как ионы благородных металлов, обладают сильными окислительными свойствами. Из растворов PtCl4 при действии избытка восстановителей выделяется платина. Ионы благородных металлов характеризуются исключительно выраженной способностью к комплексообразованию. Из большого числа комплексных соединений платины в лабораторной практике находит применение, как реактив на ион калия, платинохлористоводородная кислота. [7]
Например, ионы палладия легко гидролизуются, образуя малорастворимую коллоидную гидроокись при рН 7 5 из солянокислого раствора и при рН 2 5 из сернокислого или хлор-нокислого растворов. Кроме того, для осаждения на поверхности каталитически активных металлов используют их коллоидные растворы и растворы в органических растворителях. [9]
Проведению реакции мешают ионы палладия, золота и рутения. [10]
Проведению реакции мешают ионы палладия, а также большие количества ионов золота и рутения. [11]
Подобно иону никеля ион палладия ( II) имеет координационное число 4 по отношению к диметилглиоксиму ( H2D) и образует плоский квадратный комплекс, нерастворимый в воде. Однако в отличие от диметилглиокси-мата никеля диметилглиоксимат палладия устойчив в кислых растворах, а в щелочной среде растворяется, проявляя способность к дополнительной координации гидроксил-ионов. В щелочной среде в присутствии окислителя никель образует с диметилглиоксимом красный растворимый в воде комплекс [30]; на этом свойстве основывается фотометрический метод определения никеля. Комплексу приписывают формулу [ Ni ( D) 3 ] 2 -, где никель четырехвалентен. В качестве окислителя чаще всего применяют бромную воду, персульфат или иод. [12]
Проведению реакции мешают ионы палладия, золота и рутения. [13]
Реакции мешают только ионы палладия. Поэтому их предварительно связывают диметилглиоксимом, для чего в капельной пробирке к 0 2 - 0.8 мл испытуемого раствора прибавляют несколько крупинок диметилглиоксима и встряхивают около 1 мин. После этого кончиком капилляра берут 0 05 мл прозрачного раствора и проводят реакцию на ион золота. [14]
С увеличением концентрации ионов палладия и гипофосфита стабильность раствора уменьшается, а с увеличением рН среды несколько увеличивается. Увеличение концентрации пирофосфата натрия приводит к уменьшению скорости палладирования, но увеличивает стабильность раствора. Для ускорения процесса химического палладирования рекомендуется вводить в раствор фторид аммония. [15]
Страницы: 1 2 3 4
