Ион - большинство - металл
Cтраница 1
Ионы большинства металлов вступают в растворе в реакцию комплексообра-зования с различными ионами и молекулами. В качестве лигандов могут выступать молекулы растворителя ( воды), ионы гидроксония и гидроксила, анионы и катионы, молекулы и ионы органических соединений. [1]
Ионы большинства металлов образуют с присутствующими в растворах ионами и молекулами комплексы, состав и строение которых зависят от природы и. Комплекс, содержащий один ион металла, называют одноядерным; если в состав комплекса входит два или большее число ионов одного или разных металлов, его называют многоядерным. Частицы, непосредственно связанные с металлом, образуют внутреннюю координационную сферу комплекса; их называют внутрисферными лигандами. Металл и многоатомный лиганд обычно связаны через один или большее число донорных атомов, которые содержат неподеленные пары электронов, используемые для образования двухцентровой химической связи. При координации металлом молекул, содержащих кратные связи, могут образовываться трехцентровые и многоцентровые связи. [2]
Однако ионы большинства металлов ( Mg2, Ni2, Co2 и многие другие) в результате частичного гидролиза образуют с СО § - в водном растворе не средние, а основные карбонаты, которые могут содержать кристаллизационную воду. [3]
Однако ионы большинства металлов ( Mg2, Mi2, Со2 и многие другие) в результате частичного гидролиза образуют с СО2 - в водном растворе не средние, а основные карбонаты, которые могут содержать кристаллизационную воду. На состав основных карбонатов влияют также условия высушивания их осадков. [4]
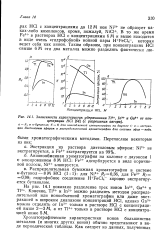 |
Зависимости характеристик удерживания Т13, / п и Ga3 от концентрации НС1 ( с разрешения автора. [5] |
Хроматографические характеристики ионов большинства металлов ( и многих других ионов) обычно представляют в виде периодической таблицы. [6]
Мурексид взаимодействует с ионами большинства металлов, поэтому перед определением кальция следует отделить металлы I - III аналитических групп. [7]
Удивительнее должно показаться то обстоятельство, что ионы большинства металлов, включая А13 и ионы переходных металлов, образуют слабо кислые растворы. Пока что мы оставляем этот факт без объяснения, но еще вернемся к его обсуждению в разд. [8]
Метод наиболее пригоден для очистки солей магния, никеля и кобальта, так как гидроксиды этих металлов осаждают ионы большинства металлов. [9]
Метод наиболее пригоден для очистки солей магния, никеля и кобальта, так как гидроокиси этих металлов осаждают ионы большинства металлов в виде их гидроокисей. [10]
Метод наиболее пригоден для очистки солей магния, никеля и кобальта, так как гидроксиды этих металлов осаждают ионы большинства металлов в виде их гидроксидов. [11]
Как видно пз приведенного ряда, метод этот наиболее пригоден для очистки солой магния, никеля и кобальта, так как гидроокиси этих металлов осаждают ионы большинства металлов в виде их гидроокисей. [12]
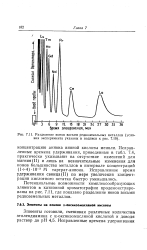 |
Разделение ионов восьми редкоземельных металлов ( условия эксперимента указаны в подписи к. [13] |
Исправленные времена удерживания, приведенные в табл. 7.4, практически указывают на отсутствие изменений для магния ( II) и лишь на незначительные изменения для ионов большинства металлов в интервале концентраций ( 1 - М) - 10 - 3 М тартрат-аниона. Исправленное время удерживания свинца ( II) по мере увеличения концентрации кислотного остатка быстро уменьшалось. [14]
Как видно из приведенного ряда, метод этот наиболее пригоден для очистки солей магния, никеля и кобальта, так как гидраты окисей этих металлов осаждают ионы большинства металлов в виде их гидроокисей. [15]
Страницы: 1 2