Вычисление - изменение
Cтраница 1
Вычисление изменений изохорного и изобарного потенциалов процессов с целью предсказания направления этих процессов является одной из важнейших задач химической термодинамики. [1]
Вычисление изменения энергии системы в МК-алгоритме является самым длительным по времени шагом. Вероятности переходов системы не нуждаются в вычислении; они могут быть запомнены в справочной таблице для облегчения доступа к ним. [2]
Вычисление изменения шнцентрации ионов при добавлении небольшого избытка одного из них опять проще всего выполняется графическим путем. [3]
Вычисление изменения изобарного потенциала производится по уравнению ( 41), глава II. Однако это уравнение не дает информации о скорости реакции. [4]
Вычисление изменения свободной энергии, связанного с реакцией, позволяет рассчитать положение равновесия для реакции и служит признаком осуществимости данного химического процесса. Положительное значение ДС накладывает ограничение на предел, до которого может дойти реакция. Заметно отрицательное значение Д ( 30 указывает, что реакция термодинамически предпочтительна. [5]
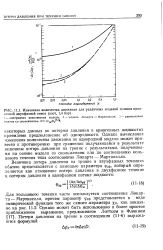 |
Изменение количества движения для различных моделей течения криогенной двухфазной смеси ( азот, 1 4 бар. [6] |
Однако вычисление изменения количества движения по однородной модели может привести к противоречию при сравнении получающейся в результате величины потерь давления на трение с результатами, полученными на основе модели со скольжением или по соотношению кольцевого течения типа соотношения Локарта - Мартинелли. [7]
Методы вычисления изменения энтальпии, сопровождающего данное физическое или химическое превращение при любых заданных условиях температуры и давления, уже рассмотрены выше. Хотя в дальнейшем мы рассмотрим и другие методы вычисления AZ, но непосредственное применение для этой цели уравнения (6.1) открывает наиболее широкие возможности во всех областях химии и дает, невидимому, наиболее точные результаты. [8]
Метод вычисления изменения энтальпии реакции зависит прежде всего от эмпирических данных теплот образования и теплот сгорания ( см. гл. Имеются различные эмпирические методы для определения теплот образования. Такие методы применяют, когда нет прямых экспериментальных данных. Данные по тепло-там образования и теплотам сгорания обычно относятся к 25 С и 1 атм. [9]
Результаты вычислений изменения свободной энергии в зависимости от температуры для рассматриваемых реакций представлены в таблице, из которой следует, что в интервале температур 200 - 1000 все приведенные реакции обладают достаточно большими отрицательными значениями-свободной энергии ( - AZ), что свидетельствует о возможности протекания реакций. [10]
Перед вычислением изменения энтальпии необходимо определить количество воздуха и газообразных продуктов сгорания - Для полного окисления одного моля метана требуется минимум два моля кислорода. Получается один моль двуокиси углерода и два моля водяного пара. Так как кислород получен из атмосферы, то ( 79 / 21) - 2, 4 9 03 моля азота также входят в систему в потоке воздуха и покидают ее с газообразными продуктами сгорания. Эти величины суммированы следующим образом. [11]
При вычислении изменения параметров разработки во времени принимается, что все скважины имеют один и тот же коэффициент продуктивности, равный 1 17 м3 / сутки am, и дебиты 6 35 м3 / сутки. Ввиду больших эксплуатационных расходов экономический предел для дебита скважины выбирается снова равным 0 8 м3 за календарные сутки. [12]
 |
К вычислению изменения напряжения в двухобмоточном трансформаторе. [13] |
При вычислении изменений напряжения трехобмоточного трансформатора коэффициенты нагрузки и коэффициенты мощности вторичных обмоток kz и cos ф2 и k3 и cos ф3 обычно заданы, a k1 и cos фг нужно вычислить. Из формул ( 2 - 13) - ( 2 - 18) видно, что - при вычислении изменения напряжения трехобмоточного трансформатора можно обойтись без вычисления kl и cos фх. Однако эти коэффициенты понадобятся ниже, и мы дадим здесь их вычисление. [14]
Значительно сложнее вычисление изменения шестого эллиптического элемента - времени прохождения перигея. [15]
Страницы: 1 2 3 4