Ион - одинаковая валентность
Cтраница 2
Из двух веществ с ионами одинаковой валентности более склонно к переохлаждению то, у которого радиус ионов меньше. Присутствие ОН-группы у органических веществ также благоприятствует переохлаждению. [16]
При обменных реакциях между ионами одинаковой валентности гистерезис не наблюдается. [17]
Практически удобно считать коэффициенты активности ионов одинаковой валентности примерно равными, если одинаковы ионные силы растворов. [18]
Из уравнения видно, что при обмене ионов одинаковой валентности обменная способность ионита не зависит от разбавления. При обмене же ионов разной валентности поглощение ионов с большей валентностью увеличивается по мере разбавления растворов. Эта закономерность подтверждена экспериментально на различных конденсационных ц полимерпзационных ионитах независимо от числа поперечных связей и активных групп. [19]
В том случае, когда в ионообменной колонке перемещаются ионы одинаковой валентности, расположение компонентов не зависит от концентрации вводимого в колонку раствора. Если же в колонке движется система ионов разной валентности, то порядок их следования зависит также и от концентрации ( II, 60) и может быть изменен на обратный путем простого изменения концентрации вводимого в колонку раствора. Подобная инверсия сорбционных рядов ионов наблюдается как при вытеснительной, так и при элютивной ионообменной хроматографии. [20]
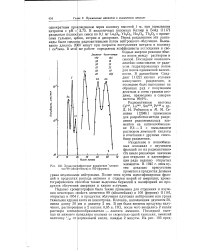 |
Хроматографическое разделение элементов 99 ( эйнштейния и 100 ( фермия. [21] |
Последние оказались линейно зависящими от радиусов гидратированных ионов для ионов одинаковой валентности. [22]
При высокой температуре в неводных средах или при высоких концентрациях обменные потенциалы ионов одинаковой валентности с ростом атомного номера не увеличиваются, а остаются такими же или даже уменьшаются. [23]
Использование величины радиуса гидратированных ионов для оценки селективности их адсорбции возможно лишь при сравнении ионов одинаковой валентности и одинаковом строении их внешних электронных оболочек. В противном случае влияние величины заряда иона и его поляризуемости может оказаться фактором, перекрывающим влияние величины радиуса иона. [24]
Необходимо отметить, что в отдельных случаях имеет место инверсия компонентов в ионообменной хроматографии также и для ионов одинаковой валентности. [25]
Полученные ряды свидетельствуют о том, что сорбционная способность определяется прежде всего зарядом ионов, а в ряду ионов одинаковой валентности повышается по мере уменьшения энергии активации молекул воды в ближнем окружении ионов. [26]
Указанное определение произведения растворимости соответствует тому случаю, когда соли взаимной пары при распадении дают по одной паре ионов одинаковой валентности. Несколько иной способ подсчета применяется для растворов разновалентных солей. [27]
Полученные ряды свидетельствуют о том, что сорбционная способность определяется прежде всего зарядом ионов, а в ряду ионов одинаковой валентности повышается по мере уменьшения энергии активации молекул воды в ближнем окружении ионов. [28]
Ионообменное равновесие является предметом изучения многих теоретических и экспериментальных работ из которых большая часть относится к изучению равновесия обмена ионов одинаковой валентности. Между тем изучение закономерностей обмена разновалент-ных ионов представляет как теоретический, так и практический интерес. Имеющиеся в литературе отдельные сообщения [1-6] о равновесии обмена той или иной пары ионов разной валентности показывают, что равновесное распределение сильно изменяется в зависимости от концентрации и состава раствора, свойств обменивающихся ионов и смолы. [29]
Однако следует отметить, что эти эффекты в основном исследованы для процесса взаимного растворения твердых тел без кристаллизации новой фазы и для случая, когда диффундируют атомы или ионы одинаковой валентности. Но в данном случае в результате такой встречной диффузии катионов происходит образование новой фазы и положение исходной границы раздела MeO / Fe2O3 будет уже определяться не только соотношением встречных потоков, но и разницей мольных объемов новой и исходных фаз. [30]
Страницы: 1 2 3 4