Ион - ванадий
Cтраница 3
Интересно, что ионы ванадия ( IV) не восстанавливаются гидразином даже при повышении температуры до 800 С. [31]
 |
Структура ванадиевой бронзы. [32] |
В лятиокиси ванадия ион ванадия расположен в координации квадратной пирамиды [333], а под влиянием иона Мо6 образуются бипирамиды, соприкасающиеся ребрами. Наличие двух этих групп указывает яа образование ванадиевых бронз типа MeV Oio, решетка которых состоит из соприкасающихся друг с другом квадратных пирамид. [33]
В последнем случае ионы ванадия, пЬ - видимому, замещают ионы кадмия и образуют октаэдриче-скую координацию ионов хлора. [34]
Предложен метод разделения ионов ванадия ( IV) и ( V) и железа ( III) колоночной распределительной хроматографией с обращенной фазой с использованием в качестве экстрагента неразбавленного ТБФ. Разделение возможно в присутствии 100-кратного избытка сульфат-ионов. [35]
Сафранин в присутствии ионов ванадия ( II) обесцвечивается. При титровании избытка этих ионов раствором железо-аммонийных кзасцов в момент завершения реакции, при появлении в растворе минимального избытка окислителя ( ионов трехвалентного железа) вновь появляется красная окраска сафранина, что указывает на окончание титрования. [36]
Катодные хронопотенциограммы восстановления ионов ванадия ( V), селена ( IV) и теллура ( IV) хорошо выражены. [37]
Вышеизложенный материал по состоянию ионов ванадия ( П Ш 1У) в водных растворах нами был для наглядности представлен в виде диаграммы областей существования ионов ванадия как функции рН и общей концентрации последнего ( рис. 2), а в табл. 2 привели возможные ионные равновесия ванадия низших степеней окисления, полученные на основании данных потенциометрического метода. [38]
В статье рассматривается взаимодействие ионов ванадия с различными гвдроксамовыми кислотами и механизм образования комплексов в зависимости от их строения. Произведено сопоставление чувствительности и условий образования комплексов ванадия гидроксамо-выми кислотами. Показаны оптимальные условия образования соединений ванадия с гвдроксамовыми кислотами. Показано, что для аналитических целей перспективно использование бензгидроксамовой, сали-цалгидроксамовои и М - толилциннамоилгидроксамовой кислот. [39]
Через 5 мин избыток ионов ванадия ( II) оттитровывают раствором железоаммонийных квасцов с сафранином в качестве индикатора. [40]
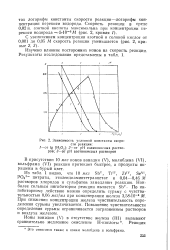 |
Зависимость условной константы скорости реакции. [41] |
В присутствии 10 мкг ионов ванадия ( V), молибдена ( VI), вольфрама ( VI) реакция протекает быстрее, а продукты окрашены в бурый цвет. [42]
Метод основан на осаждении ионов ванадия ( V) из уксуснокислого раствора ацетатом свинца. [43]
Ионы молибдена открываются аналогично ионам ванадия и вольфрама с церулеином [125] по желтому свечению. [44]
В системе с ванадием два иона ванадия образуют двух-ядерный комплекс с азотом, а два другие иона ванадия передают дополнительно два электрона на активированный азот. [45]
Страницы: 1 2 3 4