Ион - четырехвалентный ванадий
Cтраница 1
Ионы четырехвалентного ванадия в кислых растворах очень устойчивы и не окисляются кислородом воздуха даже при температуре кипения. [1]
Появляется чисто голубая окраска, свойственная ионам четырехвалентного ванадия. Таким образом, зеленая окраска обусловлена одновременным наличием в растворе ионов ванадила голубого цвета и остатков иода желтого цвета. Если продолжать кипячение, то вновь начинается выделение иода и раствор буреет, причем бурая окраска сохраняется даже при выпаривании раствора почти досуха. Были также постав - Лены количественные опыты с улавливанием и титрованием выделяющегося иода, которые подтвердили; что восстановление ванадия по схеме V - V3 начинается лишь после того, как почти весь иод, образовавшийся в результате процесса Vм - V, будет отогнан. [2]
Раствор феррованадия окрашен в голубой цвет ионами четырехвалентного ванадия. Его окисляют броматом калия, как описано в предыдущем опыте. Из полученного таким образом раствора осаждают едким натром гидроокись железа, отделяют раствор от осадка и переносят его в другой конус. Здесь выполняют реакцию с 8-оксихинолином, наблюдая образование тем-ного осадка. [3]
Раствор феррованадия окрашен в голубой цвет ионами четырехвалентного ванадия. [4]
Россотти [26] спектрофотометричесним и потен-циометрическим методами было исследовано поведение ионов четырехвалентного ванадия в ЗМ растворе перхлората натрия. [5]
Взаимодействие бромпирогаллового красного, алюминона и алюмокрезона - с ионами четырехвалентного ванадия. [6]
Церк овницкая И.А. Взаимодействие бромпирогаллового красного, алюминона и алшокрезо-на с ионами четырехвалентного ванадия. [7]
Отношение / 4 / У0бщ возрастает с 0 045 при х / у 1 до 0 378 при х / у 200, и поэтому было выдвинуто предположение, что ионы четырехвалентного ванадия присутствуют в стекле в виде ионов ванадила VO2, которые являются модификаторами. Это противоречит предположению Мунаката [27], который считает, что ионы V4 и V5 должны занимать эквивалентные позиции в структуре стекла, иначе не произойдет переноса электронов, обусловливающего электропроводность. [8]
Золотухин [3] считает, что VO2 образует с сег-нетовой солью соединение с соотношением компонентов 2: 1, а А. В. Павлинова [4] колориметрическим и криоскопическим методом установила, что в соединении, образующемся в растворе в слабощелочной среде между ионом четырехвалентного ванадия и тартрат-ионом, на один атом ванадия приходится две молекулы тартрата. Автор отмечает высокую стабильность этих соединений. [9]
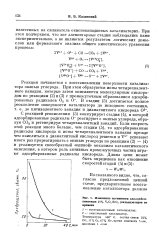 |
Изменение активности ванадийси-ликатных ( 1 % V2O5 SiO2 ( катализаторов во времени. [10] |
С реакцией реокисления ( 5) конкурирует стадия ( 4), в которой адсорбированные радикалы 0 - реагируют с окисью углерода, образуя С02 и регенерируя четырехвалентный ванадий. Если скорость этой реакции много больше, чем стадии ( 5), то адсорбированные радикалы кислорода и ионы четырехвалентного ванадия прежде чем окислиться в диамагнитный кислород решетки и V5 1 успевают много раз прореагировать с окисью углерода по реакциям ( 2) - ( 4) и реализуется своеобразный цепной механизм каталитического окисления, в котором роль активных промежуточных частиц играют адсорбированные радикалы кислорода. [11]
Своеобразный - метод электроосаждения ванадия предлагают А. С. Гончаренко и О. А. Суворова 1268 - 272 ]: при электролизе щелочных растворов ванадата на катоде происходит восстановление пятивалентного ванадия до четырехвалентного, который образует с невосстановившимся пятивалентным ванадием практически нерастворимый ванадил-ванадат. Таким образом, процесс сводится к электролитической регулировке рН раствора и к химической реакции в растворе с участием электролитически восстановленного иона ванадия, причем на один ион четырехвалентного ванадия в составе осадка приходится до 6 ионов пятивалентного. [12]
Цепи состоят из тетраэдров Р04 и V04, один из атомов кислорода которых односторонне связан с атомом ванадия или фосфора двойной связью ( точно та: же, как в тетраэдрах пятиоксидов ванадия и фосфора [203]), два других образуют мостики, связывающие атомы фосфора и ванадия в цепочку ( что совершенно аналогично цепочкам в пятиоксиде ванадия) и, наконец, четвертый атом кислорода идет на связывание в данном случае, видимо, щелочного металла, а в случае двухкомпонентного стекла V205 - P205 он образует мостиковую связь с соседней цепочкой. Очевидно, цепочки в стекле создают различные неправильные гетеродесмические образования, связанные между собой в основном ван-дер-ваальсовыми силами и отдельными сшивками из ковалентных связей. Что касается ионов четырехвалентного ванадия, всегда присутствующих в стекле, то, как полагают авторы работы [490], они находятся там в виде ионов ванадила VOJ, которые являются модификаторами. Это противоречит предположению [491], в соответствии с которым ионы V4 и V5 должны занимать эквивалентные позиции в структуре стекла, так как иначе не произойдет переноса электронов, обусловливающего электропроводность. [13]
Интересно отметить, что ИК-спектры экстрактов V ( III) и V ( IV) идентичны. Это обстоятельство также подтверждает мнение, высказанное в литературе [1], о том, что строение тройных комплексов зависит от характера взаимодействия отдельных элементов с кислородом карбонильных групп, а уменьшение или увеличение ковалентности образующейся донорно-акцепторной связи влияет на прочность соединений. Как известно, ионы трех-и четырехвалентного ванадия отличаются склонностью к образе-ванию координационной связи через кислородные атомы групп адденда. [14]
Все соединения содержат в своем составе группу VO, которая придает растворам голубой цвет и остается неизменной в ходе различных химических реакций. Рентгеноструктурный анализ соединений ванадила [20] показывает, что ион ванадила представляет собой искаженный октаэдр, где одна связь вУ 0 короче других. Это можно объяснить следующим образом: ион четырехвалентного ванадия содержит только один d - электрон который может оставаться в основном состоянии на уровне с Я 2, тогда как образование У - и 3t - связей, которое увеличивает энергию пустых орбита-лей с Я 0 и I, стабилизирует комплекс. Заряд этого иона, установленный потенциометрическим методом [22], равняется двум. [15]
Страницы: 1 2