Ион - родий
Cтраница 1
Ионы родия легко восстанавливаются до металлического состояния газообразным водородом. [1]
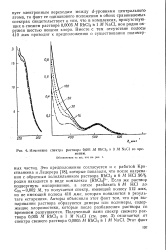 |
Изменение спектра раствора 0 001 М RhCl3 в 3 М NaCl со временем. [2] |
NaCl, ион родия окружен шестью ионами хлора. [3]
Объясняется это включением ионов родия в поверхностные узлы кристаллической ионной решетки серебра и дополнительным вытеснением соответствующего числа ионов Ag вблизи мест включения. Такие места выполняют роль эффективных ловушек электронов, конкурирующих при экспонировании с центрами светочувствительности. Вследствие этого распределение центров по светочувствительности становится избирательнее, что и приводит к существенному росту коэффициента контрастности эмульсии. [4]
ПАН образует с ионами родия ( III) в кислой или слабокислой среде при нагревании на водяной бане соединение зеленого цвета, растворимое в диметилформамиде. Кривые светопоглощения растворов соединения имеют во всей области рН существования этого соединения два максимума светопоглощения: при 590 и 630 нм. [5]
Настоящее сообщение посвящается изучению гидролиза иона родия ( III) в зависимости от рН и состава раствора. [6]
Образование комплекса одновалентного родия с малеиновой кислотой предотвращает дальнейшее восстановление иона родия до металла. [7]
Видно, что в обеих системах кривые для различных концентраций иона родия не совпадают друг с другом. Этот факт является прямым доказательством существования в растворах исследуемых систем полиядерных гидроксокомплексов. [8]
Установлена также величина IgA начала образования полиядерных гидроксокомплексов для различных концентраций иона родия. [9]
Из рассмотрения рис. 2 и 3 видно, что кривые образования для различных концентраций иона родия сдвинуты друг относительно друга по оси абсцисс Igft. А так как начало каждой кривой соответствует появлению в растворе гидроксокомплексов, то из представленных рис. 2 и 3 можно определить значение Igft ( при данных условиях эксперимента) начала образования полиядерных гидроксокомплексов. Данные, полученные таким образом, представлены в таблице. [10]
Иначе проявил себя NaRhyD, полученный другим способом, но содержащий близкое с NaRhY-255 количество ионов родия. [11]
Различие в поведении обеих систем проявляется также при сравнении величины максимального значения Z и положения кривой образования на оси gh при заданной концентрации иона родия. Отмеченные различия кривых образования систем RhCl3 - NaClO4 - H2O и Rh ( ClO4) 3 - NaClO4 - H20 можно объяснить различием форм исходных комплексов, в которых существует родий: в первой системе доминирующим является комплекс [ КпС1з ( Н2О) з ] 0, что затрудняет гидролиз и полимеризацию по сравнению со. [12]
Дальнейшее насыщение растворов с целью получения концентраций, необходимых для переработки сернокислого раствора, до продукта соответствующей реактивной квалификации приводит к тому, что наряду с переходом ионов родия в раствор происходит процесс разрыхления поверхности электрода, обусловленный обратным процессом выделения родия на электроде в отрицательный полупериод переменного тока. При этом рост концентрации соли в растворе практически прекращается. [13]
Технологическая цепочка получения рутения включает растворение платиновых концентратов в царской водке, сплавление осадка с кальцинированной содой, бурой, свинцовыми глетом и древесным углем, окислительное сплавление с серебром на пористом сосуде из огнеупорного материала ( купелирование), последующую обработку азотной кислотой, сплавление осадка с бисульфатом натрия, растворение в воде, фильтрование осадка, сплавление его с гидроокисью калия и нитратом калия или перекисью натрия, повторное растворение в воде и, наконец, выделение рутения либо пропусканием через раствор хлора, отгонкой RuC4, улавливанием иона родия смесью метилового спирта и соляной кислоты с последующим выпариванием, либо улавливанием иона родия в приемниках с соляной кислотой с последующим кипячением и обработкой хлоридом аммония. При прокаливании этих соединений в атмосфере водорода при 1273 К получают рутениевую губку. [14]
Технологическая цепочка получения рутения включает растворение платиновых концентратов в царской водке, сплавление осадка с кальцинированной содой, бурой, свинцовыми глетом и древесным углем, окислительное сплавление с серебром на пористом сосуде из огнеупорного материала ( купелирование), последующую обработку азотной кислотой, сплавление осадка с бисульфатом натрия, растворение в воде, фильтрование осадка, сплавление его с гидроокисью калия и нитратом калия или перекисью натрия, повторное растворение в воде и, наконец, выделение рутения либо пропусканием через раствор хлора, отгонкой RuC4, улавливанием иона родия смесью метилового спирта и соляной кислоты с последующим выпариванием, либо улавливанием иона родия в приемниках с соляной кислотой с последующим кипячением и обработкой хлоридом аммония. При прокаливании этих соединений в атмосфере водорода при 1273 К получают рутениевую губку. [15]
Страницы: 1 2