Выщелачивание - феррит - натрий
Cтраница 1
 |
Технологическая схема получения каустической соды ферритным способом ( отделение получения разбавленного щелочного раствора. [1] |
Выщелачивание феррита натрия осуществляется в батарее выще-лачивателей ( см. ниже) при конечной температуре щелока 95 - 100 С. [2]
Процесс выщелачивания феррита натрия осуществляется по принципу противотока. В аппарат, загруженный свежей массой феррита натрия, поступает концентрированный щелок из соседнего аппарата, а в аппарат с почти выщелочным ферритом натрия подают чистую воду. Щелок, выходящий из последнего аппарата, загруженного свежим гашеным ферритом, содержит 360 - 380 г / л NaOH и периодически перекачивается в отстойник 22 для осветления. [3]
Процесс выщелачивания феррита натрия осуществляется ио принципу противотока. В аппарат, загруженный свежей массой феррита натрия, поступает концентрированный щелок из соседнего аппарата и, наоборот, в аппарат с почти выщелоченным ферритом подают чистую воду. Щелок, выходящий из последнего аппарата ( загруженного свежим гашеным ферритом), содержит около 360 - 380 г / л NaOH. Этот щелок поступает дальше в цилиндрические резервуары 5 для осветления. Промытую окись железа из аппарата 4 возвращают в смеситель 1 для повторного использования. [4]
Процесс выщелачивания феррита натрия осуществляется по принципу противотока. В аппарат, загруженный свежей массой феррита натрия, поступает концентрированный щелок из соседнего аппарата, а в аппарат с почти выщелочным ферритом натрия подают чистую воду. Щелок, выходящий из последнего аппарата, загруженного свежим гашеным ферритом, содержит 360 - 380 г / л NaOH и периодически перекачивается в отстойник 22 для осветления. [5]
Образовавшийся при выщелачивании феррита натрия раствор, содержащий 360 - 380 г / л NaOH, поступает на концентрирование ( при получении жидкой каустической соды) или на последующее обезвоживание ( плавление) до образования твердого продукта. [6]
Отстойник слабого щелока после выщелачивания феррита натрия служит для осветления жидкости от взвешенных в ней частиц карбоната натрия и окиси железа. [7]
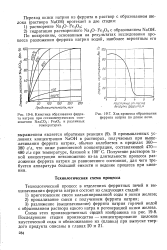 |
Кинетика образования феррита натрия при стехиометрическом соотношении Na2CO3. Рв2О3 и различных температурах.| Ход процесса образования феррита натрия по длине печи. [8] |
В промышленных условиях концентрация NaOH в растворах, получаемых при выщелачивании феррита натрия, обычно колеблется в пределах 360 - 380 г / л, что ниже равновесной концентрации, составляющей 470 - 480 г / л при температуре, близкой к 100 С. Получение растворов такой концентрации неэкономично из-за длительности процесса разложения феррита натрия до равновесного состояния, для чего требуется аппаратура большой емкости и ведение процесса при кипении. [9]
 |
Микрофотография шлифа феррита натрия Х80 ( снимок А. Н. Вишневского. [10] |
Гранулы окиси железа имеют пористую структуру и представляют собой скелет неактивной окиси железа, частично заполненный гидратированной окисью железа, получаемой в процессе выщелачивания феррита натрия. [11]
На рис. 84 приведена технологическая схема отделения получения слабого щелока, включающего операции приготовления смеси соды и окиси железа, прокаливания этой смеси с получением феррита натрия, гашения и выщелачивания феррита натрия с получением слабого щелока. [12]
 |
Вращающаяся печь. [13] |
Обычно каждая система состоит из 11 аппаратов для выщелачивания. Процесс выщелачивания феррита натрия осуществляется по принципу противотока. В аппарат, загруженный свежей массой феррита натрия, поступает крепкий щелок из соседнего аппарата и, наоборот, в аппарат с почти выщелоченным ферритом натрия подают чистую воду. [14]
Образовавшуюся окись железа отделяют от раствора едкого натра и вновь возвращают в производственный процесс, осуществляя таким образом замкнутый цикл. Полученный при выщелачивании феррита натрия раствор едкого натра ( 360 - 410 г / л) подвергают дальнейшему концентрированию и плавке для получения твердого едкого натра. [15]
Страницы: 1