Ион - тип
Cтраница 1
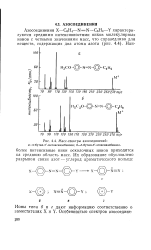 |
Масс-спектры азосоединений. а - n - бутил-я - метоксиазобензол. б-п-бутил-л - этоксиазобензол. [1] |
Ионы типа б и г дают информацию соответственно о заместителях. [2]
Ионы типа Ti3, V4 и Мп6, в которых единственный d - элек-трон находится на вырожденном уровне. Для них отклонения от октаэдрической симметрии совместно со спин-орбитальным взаимодействием приводят к очень низким значениям времени релаксации. В растворах резонанс таких соединений невозможно наблюдать, а в кристаллах он обнаруживается лишь при очень низких температурах. [3]
Ионы типа МНзСН3СОО - называют амфиона-ми, а также внутренними солями, или цвиттерионами. [4]
Ионы типа ( 7), в которых циклопропановое кольцо связано с аллильным карбониевым ионом, хотя они и хорошо изучены [13, 68], рассматриваться не будут. [5]
Ионы типа ndw ( п 1) s2 по отношению возможности образования ковалентных донорно-акцепторных связей занимают промежуточное положение между ионами подгрупп 1.1 и 1.2. Они не имеют вакантных s - орбиталей и перенос электронной плотности с донорных атомов возможен только на вакантные р-орбитали, расположенные по энергии довольно высоко. Поэтому ионы Т1 могут быть использованы при замещении в макроциклах ионов щелочных металлов, а ионы РЬ2 в некоторых отношениях напоминают ионы щелочноземельных металлов. Вследствие больших размеров этих ионов их координационные числа могут быть достаточно высокими. [6]
Ионы типа [ Re2X8jz - и их производные. В этих соединениях две квадратные группы ReX4 связаны непосредственно через атомы рения, без каких-либо мостиновых групп. [7]
Ионы типа MeL v характеризующиеся 1 войьмй ЭЛект рьнов на н ( йзрбиталях Комплексб - обраЗователя, состоящий из Четырех электронных пар, имеют конфигурацию плоского квадрата. Поэтому дЛя установления плоскоквадратного или тетраэдрического строения четырехкоординационных1 комплексов необходима дополнительная информация о магнитных свойствах: диамагн итные комплексы - плоскоквадратные, а парамагнитные - тетраэдрические. [8]
Ионы типа благородных газов можно рассматривать как простейший случай, наиболее удобный для численной обработки. [9]
Образование ионов типа U2O52 и U3O практически в этой области, как считает автор, не имеет места. [10]
Кроме ионов типа ( М2ОС1Ш) 4 - для рения известен также ион ( Re2OCli0) 3 -, в котором у атома кислорода, по-видимому, имеется один неспаренный электрон, обусловливающий парамагнетизм. [11]
Существование иона типа АЮ в парах над поверхностью кристалла подтверждено масс-спектрометрическими исследованиями. [12]
 |
Значения углов ХМХ между связями в соединениях МХз ( в градусах. [13] |
В ионах типа [ РН4 ], [ РВг4 ], [ РС14 ] и [ AsPh4 ] положительно заряженный фосфор ( изоэлектронный кремнию) и мышьяк образуют простые тетраэдрические структуры. [14]
Молекулы или ионы типа АВ7 с четырнадцатью электронами на орбиталях валентного уровня встречаются крайне редко. К ним могли бы относиться только следующие типы: АВ7, где А - элемент VII группы, ABf, где А - элемент VI группы, АВ - , где А - элемент V группы, и АВ7 -, где А - элемент IV группы. Полагают, что семь связывающих орбиталей иода относятся к одному из типов р3 3-гибридных орбиталей, хотя нельзя отрицать, что 4 / - орбитали могут играть некоторую роль в гибридизации. Даже в том случае, если вкладом 4 / - орбиталей можно пренебречь, возможны разные типы симметрии 5р3еР - гибридных орбиталей в зависимости от того, какие три d - орбитали используются. Наиболее симметричной структурой должна быть пентагональная бипирамида ( симметрия Ь5Л), и она действительно реализуется в случае IF7 как в газообразном, так и в твердом состоянии, хотя в последнем случае имеются значительные искажения. [15]
Страницы: 1 2 3 4