Ион - трехвалентный титан
Cтраница 2
Через некоторое время появляется фиолетовая окраска, свойственная ионам трехвалентного титана. [16]
Желтое комплексное соединение, образующееся при смешении титановой соли с подкисленной перекисью водорода, имеет большое значение, так как эта реакция лежит в основе весьма специфического метода анализа па перекись водорода ( см. стр. Сообщается [47], что при реакции перекиси водорода с ионом трехвалентного титана образуются свободные гидроксиль-ные радикалы, причем наблюдается легкий переход в перекисное состояние TiO... Сообщается [257], что гидрат окиси титана образует в перекиси водорода коллоидальный раствор, или гель. [17]
Содержимое пробирки осторожно нагревать до окрашивания раствора в фиолетовый цвет, характерный для иона трехвалентного титана. [18]
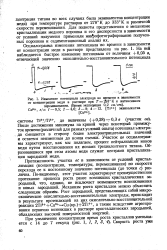 |
Изменение потенциала электрода во времени в зависимости от концентрации меди в растворе при Т 293 К и интенсивном. [19] |
После достижения минимума на кривой через некоторый промежуток времени ( различный для разных условий опыта) потенциал электро -, да смещается в сторону более электроотрицательных значений и остается неизменным до конца съемки. Участок ав осциллограммы характеризует, как мы полагаем, процесс нейтрализации ионов меди путем восстановления их ионами трехвалентного титана. Образовавшиеся при этом атомы меди служат центрами кристаллизации зародышей меди. [20]
В химических соединениях титан проявляет валентность, равную двум и трем; однако наиболее характерными для титана являются соединения с валентностью, равной четырем. Соединения двухвалентного титана в водных средах неустойчивы, легко окисляются, переходя в соединения трехвалентного, а затем и четырехвалентного титана. Ион трехвалентного титана легко образует комплексные соединения, является сильным восстановителем; в присутствии кислорода окисляется, переходя в ион четырехвалентного титана, соединения которого наиболее устойчивы. Большинство солей четырехвалентного титана являются производными не от иона ТЛ4, а от иона титанила ТЮ2, последний также является комплексообразователем. [21]
Установлено [ 241, что в этой системе через некоторое время после смешения реагентов обнаруживается узкий сигнал ЭПР. Замечено также, что наряду с реакцией восстановления четыреххлористого титана осадок, в основном состоящий из Т1С13, не дает сигнала ЭПР. Как указывают авторы, это может быть связано со слишком быстрой спин-решеточной релаксацией ионов трехвалентного титана. [22]
Установлено [24], что в этой системе через некоторое время после смешения реагентов обнаруживается узкий сигнал ЭПР. Замечено также, что наряду с реакцией восстановления четыреххлористого титана осадок, в основном состоящий из TiCl3, не дает сигнала ЭПР. Как указывают авторы, это может быть связано со слишком быстрой спин-решеточной релаксацией ионов трехвалентного титана. [23]
Комплексы TiCl3 - AlR2Cl, TiCl3 - AlRCl2 диссоциируют на A1R2C1, A1RC12 и TiCl3, который плохо растворим в углеводородных растворителях и сразу же выпадает в осадок. После выпадения осадка интенсивность сигнала ЭПР уменьшается, причем в некоторых случаях сигнал ЭПР полностью исчезает. Осадки, состоящие в основном из TiCl3 ( Al: Ti l 0), не дают сигнала ЭПР, что обусловлено, видимо, быстрой спин-решеточной релаксацией ионов трехвалентного титана. При повышенных соотношениях Al: Ti образуются осадки, дающие сигнал ЭПР. Этот сигнал обусловлен комплексами TiCla AlRCb, в которых Ti ( III) находится в кристаллическом поле измененной симметрии, что определяет возможность его наблюдения. Одновременно с этим увеличивается интенсивность сигнала ЭПР. Спектры ЭПР гептановых растворов А12Вг6, содержащих растворенный TiCls, по своей форме идентичны спектрам, характерным для систем Т1СЦ - алюминийалкил. [24]
Было обнаружено, что через определенный промежуток времени после смешения реагентов при 20 С появляется сигнал ( синглет) ЭПР. Первоначально интенсивность сигнала возрастает очень сильно, а затем, после выпадения осадка, значительно слабее. Отмечено также что выпавший осадок дает сигнал ЭПР. На основании проведенных экспериментов авторы работы приходят к заключению, что наблюдаемые сигналы ЭПР обусловлены ионами трехвалентного титана, которые образуются благодаря комплексообразованию А1 ( С. Установлено, что чем больше сила алюминийалкила как льюисов - f кой кислоты, тем больше концентрация того растворимого комплекса и тем больше интенсивность сигнала ЭПР. [25]
Кулонометрическое титрование особенно удобно при использовании нестабильных титрующих реагентов, которые можно генерировать in situ и сразу же вводить в реакцию. В этой связи представляет интерес этилендиаминтетраацетат двухвалентного железа. Шмид и Рейли [92] показали, что это соединение можно получить электрохимически из этилендиаминтетраацетата трехвалентного железа восстановлением на платиновом катоде. Окислительно-восстановительный потенциал этой пары зависит от рН, но при рН выше 2 восстановительная способность близка к соответствующему значению для ионов трехвалентного титана. [26]
Сплавление ведут до образования прозрачного плава, который выщелачивают 3 % - ным раствором серной кислоты. В полученном растворе определяют железо перманганатометрическим методом. Для этого Fe2 ( SO4) 3 восстанавливают до FeSO4 различными восстановителями. Если содержание титана небольшое, можно проводить определение железа, не отделяя титана, так как ионы четырехвалентного титана восстанавливаются только после восстановления ионов трехвалентного железа, а ионы трехвалентного титана быстро снова окисляются в четырехвалентное состояние кислородом воздуха. В анализируемом растворе допустимо до 0 02 г титановой кислоты, количество которой также не мешает определению железа. В случае присутствия большего количества титана применяют несколько иной способ определения железа. [27]
Страницы: 1 2