Ион - водород
Cтраница 3
Ионы водорода, кислород или вода являются окислителями, при наличии которых может возникать коррозия металлов при предпосылках, рассмотренных ниже. На рис. 2.1 схематически показана коррозия в присутствии ионов водорода. Ионы водорода, в роли окислителя, могут быть заменены кислородом или водой. [31]
Ион водорода в водном растворе притягивает нейтральную молекулу воды, образуя комплексный катион [ Н Н2О ] или Н3О - гидроксоний. Свойства кислот зависят от иона гидроксония, а не от иона водорода, которого практически в растворе не существует. [32]
Ионы водорода обмениваются с другими ( металлическими) катионами по правилу эквивалентности, изложенному выше ( пункт 1); с другой стороны, ионы водорода не подчиняются правилу ( пункт 3) о соответствии энергии поглощения и валентности: ионы водорода поглощаются энергичнее двухвалентных металлических ионов. Приведенные сейчас положения являются связующим звеном между кислотными свойствами почвы и ее поглотительной способностью. [33]
Ионы водорода, отличающиеся особенно высокой теплотой гидратации, в безводных кислотах, по крайней мере в большинстве случаев, если не всегда, связаны более гомеополярно, чем гетерополярно, и эта гомеополярная связь имеет заметно отличающуюся от нуля ионность ( см. стр. [34]
Ион водорода, пришедший со своим положительным зарядом, сообщает его комплексному иону аммония. [35]
Ионы водорода, катализирующие реакцию этери-фикации, ускоряют также и омыление сложных эфиров. [36]
Ион водорода, вероятно, сольватирован одной молекулой серной кислоты. Большая электропроводность растворов объясняется механизмом эстафетной передачи протона; ассоциация молекул кислоты обусловлена водородными связями. [37]
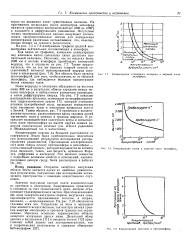 |
Концентрация атомарного водорода в верхней части экзосферы.| Концентрация ионов в верхней части экзосферь..| Концентрация протонов в протоносфере. [38] |
Ионы водорода и электроны образуются на высотах ниже 800 км в результате обмена зарядами между ионами кислорода и нейтральным атомарным водородом, а затем диффундируют кверху. Таким образом, рис. 7.9 применим к концентрациям протонов, расположенных вдоль силовых линий магнитного поля в нижних и средних широтах. [39]
Ионы водорода катализируют как прямую, так и обратную реакции. [40]
Ион водорода может, таким образом, связаться в молекулу уксусной кислоты или в молекулу воды. Ионы СН3СОО - и ОН 1 как бы конкурируют друг с другом в связывании иона водорода. Поэтому в данном случае реакция нейтрализации доходит. [41]
Ион водорода, отщепляющийся при диссоциации от карбокси. [42]
Ионы водорода из кислоты при окислительно-восстановительных реакциях обычно входят в состав воды. [43]
Ионы водорода катализируют процесс гидролиза. [44]
Ионы водорода, вернее гидроксония Н3О, нейтрализуют ионы гидрок-сила, содержащиеся в порах цементного камня, с образованием молекул воды. Высокая концентрация гидроксильных ионов, как отмечалось выше, - обязательное условие устойчивости связующих компонентов цементного камня, поэтому при рН среды ниже 12 для портландцемента без минеральных добавок и 10 5 - 11 для шлаковых цементов происходит разложение гидросиликатов и других связывающих цементного камня. [45]
Страницы: 1 2 3 4