Ион - фтор
Cтраница 3
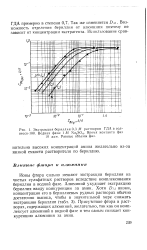 |
Экстракция бериллия 0 3 М раствором ГДА в сол. [31] |
Ионы фтора сильно мешают экстракции бериллия из чистых сульфатных растворов вследствие комплексования бериллия в водной фазе. Алюминий ухудшает экстракцию бериллия ввиду конкуренции за амин. Присутствие фтора в растворах, содержащих алюминий, желательно, так как он комплексует алюминий в водной фазе и тем самым снижает конкуренцию алюминия за амин. [32]
 |
Проекция структуры бультфонтейнита H2 ] - 2H20. [33] |
Ионы фтора не внедряются между анионами 03SiOH3 - подобно ионам ОН в структуре Caa ( HSi04) OH: в данном случае они играют роль мостиков между смежными катионными полиэдрами. [34]
Ион фтора F -, имеющий небольшую по объему и замкнутую электронную оболочку, легко делит свои электронные пары с другими атомами, образуя разнообразные комплексные соединения. К таким соединениям относятся, например, криолит Na3AlF6, в молекуле которого атом алюминия связан с шестью атомами фтора, HBF4 - кислота, в которой атом бора окружен четырьмя атомами фтора, и ряд других. [35]
Поскольку ионы фтора и гидроксила занимают в структуре воды место молекул Н2О, которые образуют химические связи по тетраэдру - две нормальные связи образуют атомы водорода данной молекулы и две связи с кислородом этой молекулы дают атомы водорода соседних молекул воды - ясно, что завышение рефракции в случае иона фтора обусловлено двумя связями О-H... [36]
 |
Слой молекул Н2О в структуре. [37] |
Один ион фтора является общим для двух октаэдров. [38]
Поскольку ионы фтора и гидроксила занимают в структуре воды место молекул Н2О, которые образуют химические связи по тетраэдру - две нормальные связи образуют атомы водорода данной молекулы и две связи с кислородом этой молекулы дают атомы водорода соседних молекул воды - ясно, что завышение рефракции в случае иона фтора обусловлено двумя связями О-H... [39]
Осаждение ионов фтора в виде фторидов кальция или свинца70, применяемое в макроанализе, не пригодно для определения малых и ничтожно малых количеств фтора, во-первых, вследствие частичной растворимости этих солей и, во-вторых, вследствие значительной влияния посторонних ионов на их растворимость. Другие весовые способы определения фтора, основанные на осаждении фтора в виде фторида висмута 71, фторида тория 72, фторида бензидина и ртути 73, фторида трифе-нилолова 74 и в виде других солей фтора75, или способы, основанные на прибавлении желатины при осаждении фторида кальция 76, также не дают точных результатов, отвечающих современным требованиям. [40]
Осаждение ионов фтора в виде фторидов кальция или свинца 70, применяемое в макроанализе, не пригодно для определения малых и ничтожно малых количеств фтора, во-первых, вследствие частичной растворимости этих солей и, во-вторых, вследствие значительного влияния посторонних ионов на их растворимость. Другие весовые способы определения фтора, основанные на осаждении фтора в виде фторида висмута 71, фторида тория 72, фторида бензидина и ртути 73, фторида трифе-нилолова 74 и в виде других солей фтора 7б, или способы, основанные на прибавлении желатины при осаждении фторида кальция 76, также не дают точных результатов, отвечающих современным требованиям. [41]
У ионов фтора электрон связан особенно прочно. Единственный метод, с помощью которого может быть освобожден электрон - это электролиз. При получении фтора встречаются некоторые экспериментальные трудности из-за его высокой реакционной способности, особенно потому, что он действует на стекло. [42]
Способность ионов фтора и гидроксила изоморфно замещать друг друга объясняется близостью их ионных радиусов. Теплота этой реакции 104 составляет 62 3 ккал / г-мол. [43]
Оттеснения иона фтора при присоединении фтористого водорода к трехфтористому бору здесь не происходит. Фтористый водород не внедряется между атомами, образующими BF3, а просто присоединяется к нему. Однако не все комплексные соединения удается однозначно распределить по этим двум классам. [44]
Радиус иона фтора равен 1 33 А, тогда как радиус ковалентно связанного атома фтора составляет 0 7 А. Таким образом, расстояния F-F в ионе ( HF2) -, хотя и различны для разных бифторидов, однако они всегда лежат между удвоенными величинами вышеуказанных радиусов. Нет достаточных оснований предполагать существование в ионе ( HF2) - связей, осуществляемых единичным электроном, как это имеет место в случае иона молекулы водорода II. Приняв для иона ( HF2) - чисто ионную структуру и проведя соответствующий расчет, Пау-линг [147] пришел к выводу, что этот ион должен иметь симметричную, линейную конфигурацию, причем расстояние между атомами фтора ( F - Н - F) должно составлять 2 32 А, что находится в соответствии с экспериментальными данными. [45]
Страницы: 1 2 3 4