Ион - хлор
Cтраница 2
Ионы хлора должны быть тщательно удалены из осадка, так как FeClg при температуре выше 315 улетучивается, что может привести к потере осадка и пониженному результату анализа. Последние 3 - 4 раза осадок промывают чистой горячей водой. [16]
Ионы хлора при небольшом их содержании в растворе не окисляются перманганатом, но в присутствии железа такое окисление происходит, и КМпО4 расходуется не только на окисление Ре - ионов, но и на окисление СР - ионов, что искажает результаты анализа. Это явление названо Н. А. Шиловым сопряженным окислением. [17]
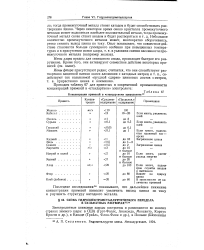 |
Концентрации примесей в стандартном электролите 27. [18] |
Ионы хлора вредны для свинцового анода, происходит быстрое его разрушение. [19]
Ион хлора является сильным активатором коррозии. Его присутствие в растворе способствует разрушению защитной пленки оксида алюминия, вследствие чего коррозия усиливается. [20]
Ионы хлора и натрия при этом выполняют функцию носителей зарядов, на их основе возможно образование щелочи NaOH и хлорного железа FeCla, или выделение газообразного хлора на аноде. [21]
Ионы хлора присутствуют почти во всех природных водах, причем содержание их изменяется в очень широких пределах. Залежи хлористых солей осадочных пород растворяются в воде и выносятся подземными водами и реками в моря и океаны, где постепенно они накапливаются, достигая высокой концентрации. Подобяо ионам Na ионы С1 - являются характерными ионами сильно минерализованных вод морей и океанов. [22]
Ионы хлора, находящиеся во всех 3 растворах, обладают одинаковыми свойствами, независимо от наличия в одном растворе ионов натрия, в другом - ионов бария, в третьем - ионов меди. [23]
Ионы хлора, несущие отрицательные заряды, имеют по лишнему электрону. [24]
 |
Схема присоединения электрона у хлора.| Схема отрывов электрона у натрия. [25] |
Ион хлора обладает иными свойствами, чем атом хлора. Атом хлора мог бы потерять свои 7 электронов внешнего слоя, в этом случае его внешний слой тоже имел бы 8 электронов, но этот процесс требует так много энергии, что практически атом хлора никогда не теряет свои внешние электроны. [26]
Ионы хлора через бетонную стенку проходят в анодную зону, а катионы Na - в катодную зону. NaOH накопить не удается, так как начинается заметная диффузия ионов ОН и коэффициент выхода по току падает. [27]
Ионы хлора в отличие от ионов калия почвой не поглощаются: они легко вымываются грунтовыми водами и уносятся в нижние горизонты. Поэтому, чтобы сохранить в почве калий, но убрать из нее хлор, нужно хлорсодержащие калийные удобрения вносить в почву осенью. Пока семена прорастут и корневая система начнет усваивать ионы из почвы, осенние дожди и талые воды успеют унести ионы хлора вглубь. [28]
Ионы хлора для разряда требуют более отрицательного потенциала, чем ионы брома, иода и родана, вследствие чего хлор, выделяющийся на аноде при электролизе водных растворов хлоридов, всегда содержит некоторое количество кислорода, так как наряду с разрядом ионов хлора протекает разряд гидроксильных ионов. [29]
Ионы хлора осаждают, прибавляя сульфат серебра, выпавший осадок отделяют на центрифуге ( фильтровать нельзя. [30]
Страницы: 1 2 3 4