Вязкость - раствор - электролит
Cтраница 1
 |
Значения коэффициента At для расчета плотности растворов солей по формуле Л. Л. Эзрохи. [1] |
Вязкость растворов электролитов специфична для каждого электролита и является функцией его концентрации и температуры раствора. [2]
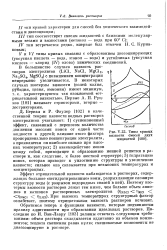 |
Типы кривых вязкости смесей двух жидкостей. [3] |
В большинстве случаев вязкость растворов электролитов ( LiCl, NaCl, MgCl2, Na2S04, MgS04) с повышением концентрации непрерывно увеличивается. Руц-ков [101] называет стрикторами, вторые - дестрикторами. [4]
 |
Сетка Дэвиса. [5] |
Для представления зависимости вязкости раствора электролита от температуры хорошо подходит диаграмма типа Дюринга. [6]
Как показывает опыт, вязкость растворов электролитов может быть как больше, так и меньше вязкости растворителя. Как известно, в этих теориях рассматриваются лишь разбавленные растворы и не учитывается молекулярная структура растворителя. Этого недостатка лишена теория Бернала и Фа-улера [2], в которой рассматривается молекулярная структура воды и влияние на нее ионов растворенного вещества. Согласно Берналу и Фау-леру, вязкость ионного раствора обусловлена следующими эффектами. [7]
 |
Результаты математической обработки кинетических кривых. [8] |
Скорость осаждения является функцией нормальности и вязкости раствора электролита, концентрации полимера в растворе и времени. [9]
 |
Алгоритм расчета динамической вязкости. [10] |
На рис. 13 показана блок-схема алгоритма расчета динамического коэффициента вязкости растворов электролитов. [11]
В данной работе следует изучить влияние температуры на электропроводность и вязкость растворов электролитов в воде пли в различных органических растворителях. [12]
В данной работе следует изучить влияние температуры на электропроводность и вязкость растворов электролитов в воде или в различных органических растворителях. [13]
Тот факт, что для растворов неэлектролитов получены разумные значения вязкости, позволяет надеяться, что, изучая вязкость растворов электролитов, можно будет сделать некоторые заключения о процессе гидратации ионов. [14]
Вязкость раствора электролита описывается уравнением Джонса - Доула: г / г 0 1 Ас112 Вс, где т) и т 0 - вязкости раствора и растворителя соответственно, А - вычисляемая постоянная, учитывающая вклад межионных сил [14, 15], В - эмпирическая константа и с - молярная концентрация. [15]
Страницы: 1 2