Ион - даюта
Cтраница 2
Таким образом, два способных восстанавливаться вида ионов дают на поляризационной кривой две волны, каждая из которых переходит в горизонтальную площадку, отвечающую предельным токам этих ионов. [16]
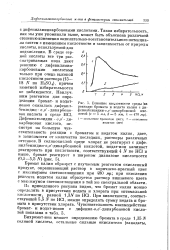 |
Влияние кислотности среды на реакцию бромата и иодата калия с ди-фенилбензидин-о о - дикарбоновой кислотой ( v 5 мл, d 5 мм, J. 470 M L. [17] |
В среде серной кислоты все три рассматриваемых иона дают реакцию с дифениламинкарбоновыми кислотами только при очень высокой кислотности раствора ( 15 - 18 N по H2S04), причем заметной избирательности не наблюдается. Дпфенилтолпдин - о о - ди-карбоновая кислота, несмотря на большую чувствительность реакции с броматом и иодатом калия, дает, в зависимости от количества последних, растворы различных оттенков. [18]
Таким образом, два способных восстанавливаться вида ионов дают на поляризационной кривой две волны, каждая из которых переходит в горизонтальную площадку, отвечающую предельным токам этих ионов. [19]
V есть ионы Zn, которые с ионами ОН дают осадок, растворяющийся при избытке этих ионов. Как следствие этого в данном опыте наблюдается частичное растворение осадка. [20]
Обнаружению части анионов мешают катионы II-V групп, которые с этими ионами дают осадки. При этом соли щелочных металлов остаются в растворе. [21]
Естественно, самая простая картина получается в том случае, когда все ионы дают одинаковое сверхтонкое расщепление. Этот случай приведен на фиг. В случае восьмерной координации правильного куба, образованного ионами фтора ( например, парамагнитный ион, замещающий ион Са2 в Сар2), отношения интенсивностей линий равны 1: 8: 28: 56: 70: 56: 28: 8: 1, если все ионы дают одинаковое сверхтонкое расщепление, так что интенсивность каждой крайней линии будет равна только Vi28 ( 1 / 2) 8 полной интенсивности. [22]
Ионы СЮз ( если они присутствуют) восстанавливаются до С1 -; С1 - - ионы дают осадок с добавленными ранее в избытке А § - ионами. [23]
Титрование проводится с вращающимся платиновым электродом при потенциале 1 0 в, так как Ре - ионы дают при этом потенциале анодный диффузионный ток, величина которого пропорциональна концентрации. [24]
Перманганаты в кристаллическом состоянии - черные вещества, их растворы имеют красно-фиолетовую окраску, причем уже ничтожные концентрации ионов MnOJ дают заметную окраску. Конечную точку титрования отмечают по установлению неисчезающей окраски КМпО4, таким образом, индикатором в данном случае является сам титрант. [25]
Пермаиганаты в кристаллическом состоянии - черные вещества, их растворы имеют красно-фиолетовую окраску, причем уже ничтожные концентрации ионов MnOi дают заметную окраску. Конечную точку титрования отмечают по установлению неисчезающей окраски КМпО, таким образом, индикатором в данном случае является сам титрант. [26]
 |
Электронные структуры катионов и аналитические группы. [27] |
Являясь сравнительно сильными поляризаторами, они в то же время заметно поляризуются сами и потому при взаимодействии с ионами S дают труднорастворимые сульфиды. Однако последние сильно различаются по своей растворимости в зависимости от положения соответствующих элементов в периодической системе элементов. Именно катионы, образованные элементами второй и третьей триад системы Менделеева Ru 1 1 1, Rh, Pd, Os, Ir, pt f относятся к IV и V аналитическим группам, как и катионы с электронными структурами 18 и 18 - Ф-2. Причиной этого является то обстоятельство, что наличие у них глубинных 18 - и 32-электронных слоев усиливает их поляризующую способность и собственную поляризуемость; усиление же поляризационных взаимодействий при соединении катионов с ионами S влечет за собой понижение растворимости соответствующих сульфидов. [28]
Являясь сравнительно сильными поляризаторами, они в то же время заметно поляризуются сами и потому при взаимодействии с ионами S дают трудно растворимые сульфиды. Однако последние сильно различаются по своей растворимости в зависимости от положения соответствующих элементов в периодической системе элементов. Причиной этого является то обстоятельство, что наличие у них глубинных 18-и 32-электронных слоев усиливает их поляризующую способность и собственную поляризуемость; усиление же поляризационных взаимодействий при соединении катионов с ионами S влечет за собой понижение растворимости соответствующих сульфидов. [29]
В растворе хлорида ванадия, полученного в опыте 8, кроме ионов V есть ионы Zn, которые с ионами ОН дают осадок, растворяющийся при избытке этих ионов. Как следствие этого в данном опыте наблюдается частичное растворение осадка. [30]
Страницы: 1 2 3 4