Двухвалентный ион - железо
Cтраница 4
Увеличение минерализации электролита в двухфазной системе ведет к росту скорости коррозии углеродистой стали. Повышение скорости коррозии в присутствии сульфата железа может быть объяснено своеобразным влиянием двухвалентных ионов железа, которые при небольшом изменении рН электролита в тонком слое способствуют более быстрому образованию на поверхности металла осадда сульфида железа, стимулирующего коррозию. [46]
Раствор содержал также малые количества феррицианида калия, который принимает синюю окраску в присутствии двухвалентных ионов железа, и фенолфталеина, который становится розовым в присутствии щелочи. Вначале синие анодные и розовые катодные участки образовывались по всей поверхности, как это видно на фиг. После того как весь кислород в капле восстанавливается, дальнейшая катодная реакция происходит главным образом по краям капли, куда легче всего поступает атмосферный кислород. Центральные щелочные участки не сохраняются, и весь центр становится анодным. Окончательное распределение анодных и катодных участков представлено на фиг. В месте встречи внутренней анодной и внешней катодной зон выпадает гидрат закиси железа, образующий кольцо внутри капли. Образование ржавчины начинается с формирования плохо растворимого Fe ( OH) 2, который затем превращается в FeO-OH, и, возможно, в другие вещества ( разд. [47]
Относительно молекулярного механизма действия третьего класса ингибиторов с общим анионом типа М02 - имеется несколько точек зрения. Эванс и Хор [1] предполагали одно время, что хромат-ионы отнимают, например, от двухвалентных ионов железа, перешедших в раствор, третий электрон, превращая их в трехвалентные ионы. [48]
Образующиеся во время спекания двухвалентные ионы железа ( особенно у ферритов, содержащих избыток Fe2O3 относительно 50 мол. Чтобы Ni-Zn - ферриты обладали хорошими высокочастотными свойствами, в их составе не должно быть двухвалентных ионов железа. Это требование можно сравнительно легко выполнить, если спекать изделия в среде воздуха, а температуру не поднимать выше 1220 С. Если спекание Ni-Zn - ферритов происходит при высоких температурах ( выше 1220 С) и при этом необходимо препятствовать образованию даже небольших количеств Fe2, то рекомендуется осуществлять спекание в среде кислорода. [49]
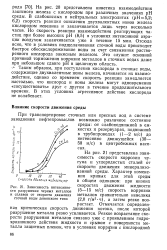 |
Зависимость интенсивно - / с г ] с ч. [50] |
На рис. 20 представлена кинетика взаимодействия закисного железа с кислородом при различных значениях рН среды. В слабокислых и нейтральных электролитах ( рН 5 2; 6 2) скорость реакции окисления двухвалентных ионов железа кислородом невелика и заканчивается лишь через несколько часов. Но скорость реакции взаимодействия реагирующих частиц при более высоких рН ( 8 5) в условиях интенсивной аэрации воздухом заканчивается уже в течение 15 мин. Отсюда ясно, что в условиях подщелачивания сточной воды происходит быстрое обескислороживание воды за счет связывания растворенного кислорода закисным железом. Это служит основной причиной торможения коррозии металлов в сточных водах даже при небольшом сдвиге рН в щелочную область. Таким образом, при поступлении кислорода в сточные воды, содержащие двухвалентные ионы железа, начинается их взаимодействие, однако со временем скорость реакции замедляется настолько, что кислород и ионы железа могут одновременно сосуществовать друг с другом в течение продолжительного времени. В этих условиях агрессивное действие кислорода не ослабевает. [51]
 |
Цементация меди из растворов. [52] |
Основным отличием электролиза в схеме гидроэлектрометаллургии меди от электролитического рафинирования, кроме выделения кислорода на аноде, является присутствие значительного количества солей железа в растворе, и борьба с их влиянием. Дело в том, что на нерастворимом свинцовом аноде при высокоположительном его потенциале ( § 37) возможно окисление двухвалентных ионов железа до трехвалентных ( окислительно-восстановительный потенциал этого процесса равен 0 75 в), и потому в растворе всегда присутствуют соли окисного железа, растворяющие медный катод. Небольшие количества железа, попеременно восстанавливающиеся на катоде и окисляющиеся на аноде, дают значительное снижение выходов по току. Следует держать железо в состоянии закисного сульфата и по возможности не допускать его к аноду. [53]
Мп, не повысивших своей валентности, занимает тетраэдрические позиции. Между двухвалентными ионами железа, находящимися в октаэдрических позициях, и трехвалентными ионами марганца осуществляется электронная реакция типа Fe2 Mn3 Fe3 Mn2, вследствие чего уменьшается количество двухвалентных ионов железа, причем при х 0 2, по-видимому, почти все ионы железа находятся в трехвалентном состоянии. В результате удельное сопротивление достигает максимального значения. [54]
 |
Схемы массопереноса через слой QdaFejOia. [55] |
По-видимому, образование гексагональной структуры феррита бария происходит в результате диффузии ионов бария в кислородный слой оксида железа. При избытке в шихте ионов бария против стехиометрии происходит более полное замещение слабо связанных ионов кислорода в структуре Fe2O3, которое вызывает при зарядовом перераспределении изменение валентности ионов железа, а именно, появление двухвалентных ионов железа. [56]
В последнее время большое внимание уделяют изучению влияния условий термической обработки на дезаккомодацию выпускаемых промышленностью марганец-цинковых ферритов. В качестве примера можно привести работу [24], из которой следует, что величина дезаккомодации неоднозначно связана с концентрацией Fe2 и в зависимости от исходного состава ферритов может увеличиваться, уменьшаться или оставаться практически неизменной при монотонном изменении концентрации двухвалентных ионов железа; величина дезаккомодации исследованных ферритов однозначно определяется парциальным давлением кислорода при спекании. [57]
Весьма эффективным представляется использование постоянного тока для таких процессов химического растворения, на которые существенно влияют продукты электролиза. При величине потенциала на графитовых электродах, находящихся в суспензии, порядка 0 8 В скорость растворения возрастает в 2 5 - 3 раза и увеличивается степень извлечения марганца. При добавлении в раствор двухвалентных ионов железа эти показатели возрастают на порядок, что обусловлено каталитическим действием железа. [58]
Грунтовая коррозия имеет свои особенности. Вследствие этих особенностей условия катодного и анодного процессов сильно отличаются от электрохимической коррозии в протекающей воде. При грунтовой коррозии анодный процесс представляет собой переход двухвалентного иона железа в почвенный электролит, которого может не быть в сухих грунтах из-за недостатка влаги на поверхности металла; в катодном процессе происходит ассимиляция а катодных участках кислорода с переходом его в ионное состояние. [59]
Страницы: 1 2 3 4