Индивидуальный ион
Cтраница 2
 |
Стандартные термодинамические функции гидратации индивидуальных ионов при 298 К, кДж / моль. [16] |
Данные о стандартных энергиях Гиббса переноса индивидуальных ионов между растворителями традиционным путем получают разделением значений AGnep для электронейтральной комбинации ионов на ионные составляющие. [17]
В результате этого смещения уменьшается число индивидуальных ионов, повышается вероятность образования ионных двойников и более сложных ионных комплексов ( см. ниже), уменьшается электропроводность и появляется аномальная проводимость. [18]
Предложенное ими уравнение для расчета теплоты гидратации индивидуальных ионов включает ряд членов, главными из которых являются: член, отражающий взаимодействие между ионом и диполем воды в первичной гидратной оболочке; борновский член, описывающий взаимодействие первично сольватированного иона с окружающей средой; член, учитывающий взаимное отталкивание молекул в гидратной оболочке. Расчет Бернала и Фаулера очень приближенный, содержит многочисленные допущения и сейчас представляет в основном исторический интерес, поскольку является первым комбинированным методом расчета энергии сольватации ионов. Одними из применяемых в настоящее время комбинированных методов являются расчет теплоты гидратации ионов, выполненный Эли и Эвансом [80], основанный на аналогичной модели сольватации, и метод Фервея [81], в котором детально учтена ( насколько это было возможно в сороковых годах) ориентация молекул воды в первой гидратной оболочке. [19]
В первую очередь надо знать химические потенциалы индивидуальных ионов и молекул, но для более глубокого понимания механизмов ионных процессов требуются данные и по энтальпиям, и по энтропиям сольватации индивидуальных ионов. [20]
Наконец, надежное определение термодинамических функций состояния индивидуальных ионов в растворах необходимо для развития строгой теории растворов, уровень развития которой для неводных растворов существенно ниже, чем для водных. [21]
Для прямого определения стандартной энергии Гиббса сольватации индивидуальных ионов наиболее надежным считается метод Рэндлса [31], в котором измеряют разности потенциалов между ртутным электродом и водными растворами КС1 в гальваническом элементе, где контакт осуществляется через газовую фазу. Далее путем построения циклов Борна рассчитывают свободные энергии гидратации К и ряда других ионов. Гиббса гидратации ионов, которые в настоящее время считаются наиболее близкими к действительности. [22]
Сущность такого подхода к определению AG ep индивидуальных ионов состоит в том, что вместо исследования реального переноса иона из растворителя А в растворитель В ( сопряженного с большими экспериментальными трудностями и необходимостью учета межфазного потенциала) исследуется равновесие ступенчатой реакции замещения молекул сорта А на молекулы сорта В в координационной сфере иона при изменении состава смешанного растворителя А В. [23]
 |
Стандартные энергии Гиббса образования различных веществ при 298 К. [24] |
Растворенные вещества, включая электролиты, неэлектролиты и индивидуальные ионы, находятся в стандартном состоянии, если их активность равна единице, а давление равно одной атмосфере. [25]
Существует несколько методов расчета химических нулевых коэффициентов активности индивидуальных ионов. [26]
Следует отметить, что скорость k относится к индивидуальному иону с внутренней энергией Е и она не эквивалентна скорости обычной химической реакции в растворе, которая является результатом равновесных процессов с участием миллионов молекул. [27]
При более высоких значениях ионной силы различия между индивидуальными ионами становятся настолько большими, что они не допускают применения среднего приближенного значения коэфициента активности. [28]
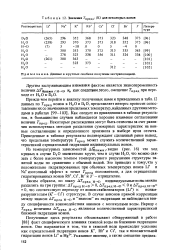 |
Значения Гпред ( К для некоторых ионов. [29] |
Таким образом, по знаку АТпрея H - D индивидуальные ионы можно разделить на три группы: ДГпред H D 0, ДГпред H-D 0 и ДГпред h - d 0, что соответствует переходу от ионов-стабилизаторов ( Li) к ионам-разрушителям ( К - Cs) структуры. В случае анионов прямой корреляции между знаком ДТ ред h - d и знаком их гидратации не наблюдается ввиду специфичности взаимодействия анионов с молекулами воды. Наряду с Тпред величины Д пред h - d являются количественной характеристикой ближней гидратации ионов. [30]
Страницы: 1 2 3 4