Перечисленный ион
Cтраница 1
Перечисленные ионы обладают сравнительно высокими потенциалами появления. [1]
Перечисленные ионы образуют также большую часть ионных кристаллов, которые рассматриваются в этом - курсе. Следует хорошо запомнить названия и формулы этих ионов, и в этом отношении очень полезно обращаться к периодической системе. [2]
Перечисленные ионы обладают сравнительно высокими потенциалами появления. [3]
 |
Характеристика люминесцирующих пленок, содержащих таллий. [4] |
Все перечисленные ионы, так же как и ионы таллия, образуют люминесцирующие кристаллы с иодидом аммония. Ионы серебра и золота ( I) не мешают открытию ионов таллия, так как для получения их люминесцирующих кристаллов, необходимо соблюдать определенные условия. [5]
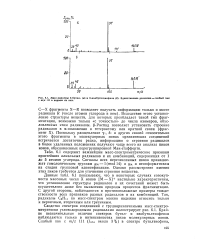 |
Масс-спектры 2-бутил - ( а и 2-изобутилтиофена ( ff. Единственное различие - слабый пик с mjx 111 в первом из них. [6] |
Сигналы всех перечисленных ионов принадлежат гомологическим группам г / м - 1 ( mod 14) и г / м и неинформативны на стадии групповой идентификации. Однако рассмотрение именна этих пиков требуется для уточнения строения вещества. [7]
Очень низкие концентрации перечисленных ионов определять трудно, так как при работе с малыми значениями генераторного тока кривая потенциометрической индикации становится плоской, что сразу снижает точность анализа. [8]
ОС, соответствующие перечисленным ионам. Разделив далее разницы в ЭПИН и ОС на 10 равных частей, можно вычислить изменение размеров галогенов и халькогенов в пределах от нуля до максимального отрицательного заряда. [9]
Практически для каждого из перечисленных ионов металлов может быть разработан метод потенциометрического определения с использованием, вообще говоря, лишь двух электродов - фторидного и сульфидного ( или иодидного) ионоселективных электродов. [10]
Более чувствительные реакции с перечисленными ионами дает висмутол II, чаще применяемый для их фотометрического определения. [11]
 |
Реакции образования кристаллофосфоров на СаО. [12] |
Открытие ионов сурьмы в присутствии перечисленных ионов возможно только в том случае, если их абсолютное содержание в капле исследуемого раствора объемом 0 01 мл не превышает следующих максимальных количеств; 0 00104 мкг для РЬ2, 0 00002 мкг для Hg2 и Hg2 0 0025 мкг для Те2 -, Se2 -, 60 0 мкг для MoVI и 100 0 мкг для WVI. Абсолютное содержание иона Sb3 в этой капле составляет 10 - 5 мкг. [13]
Характеристические суммы, составленные из интенсивностей пиков перечисленных ионов, входящих в эти семь групп, будут характеризовать относительное содержание соответствующих гомологических рядов углеводородов в образце. Коэффициенты относительной чувствительности для каждой из групп, необходимые для количественных измерений, определялись по спектрам индивидуальных углеводородов и их смесей методом варьирования концентраций. [14]
Чтобы сделать возможным открытие железа в присутствии перечисленных ионов, когда их отношение с железом превышает предельное, необходимо раствор предварительно обогатить железом, удалив избыток мешающих ионов. Так, большой избыток ионов кобальта, никеля и хрома удаляют, действуя на исследуемый раствор смесью растворов едкого натра и концентрированного раствора аммиака. Осадок растворяют в соляной кислоте и рассматривают под микроскопом. При боль шом содержании висмута в растворе его подвергают гидролизу, разбавляя раствор. [15]
Страницы: 1 2 3 4