Разный ион
Cтраница 3
Для реакции одного лиганда с разными ионами металлов изменение энтальпии в газовой фазе может служить мерой изменения энтальпии в растворе. [31]
Для реакции одного лиганда с разными ионами металлов изменение энтальпии в газовой фазе может служить мерой изменения энтальпии в растворе. [33]
В этом случае возможно оттитровать ампе-рометрически разные ионы при их совместном присутствии в растворе. [34]
Это разрушение собственной структуры воды производят разные ионы по-разному, поэтому различна их доля энергетического вклада в общее изменение энергии. Следует также учитывать и те изменения, которые могут иметь место в молекулах воды ( растворителя) в результате их соприкосновения с заряженными частицами. Несомненно, что эти изменения для разных ионов будут различными, что также сказывается на теплотах гидратации. [35]
В этом случае можно амперометрически оттитровать разные ионы при их совместном присутствии в анализируемом растворе. Например, при совместном титровании свинца и бария нисходящая ветвь кривой соответствует уменьшению предельного тока свинца. Период титрования бария, не дающего восстановительной волны, не сопровождается изменением минимального тока, достигнутого в кон-цетнтрования свинца. В конце титрования ток вновь возрастает за счет восстановления бихромата. [36]
 |
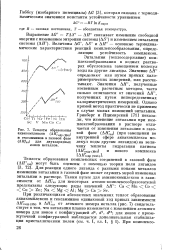
Схема уровней в жтаэдрическол.| Диаграмма уровней энер - учитывать, кроме ос-гий для конфигурации d ( ион НОВНОГО также воз. [37] |
Порядок членов может несколько варьировать у разных ионов, что связано с особенностями строения их электронной оболочки, но в основном он сохраняется для очень больших групп ионов. [38]
Так, однажды определив набор радиусов разных ионов, можно на основании данных геометрического и электростатического анализов установить, почему CsGl, NaCl и GuCl име ют разные структуры. [39]
Интересно, что в растворах стабильность разных ионов определенного типа ( первичных, вторичных, третичных) почти не зависит от строения алкильных заместителей. [40]
 |
Проточное жидкостное соединение.| Влияние концентрации соединительного раствора КС1 на потенциал ЕЛ элемента с переносом. [41] |
Экспериментальные исследования жидкостных соединений, образованных растворами разных ионов, ограничиваются в основном растворами НС1 и КС1 с применением соединительного раствора и в его отсутствие. [42]
Чтобы правильно сравнить недипольную часть взаимодействия для разных ионов, необходимо учесть тот факт, что взаимодействие в 4 / 13-ионах выражается через эффективный спин / 2 для электронного состояния, которое не является состоянием истинного спина. [43]
Чаще на ионообменной смоле адсорбируется сразу несколько разных ионов, которые затем разделяют путем пропускания через колонку растворов, отличающихся по составу от исходного раствора разделяемых ионов. В качестве таких вымывающих растворов часто используют комплек-сообразователи, образующие с отдельными ионами комплексные соединения различной устойчивости. [44]
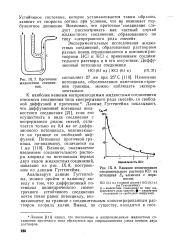 |
Влияние концентрации соединительного раствора КС1 на потенциал. д элемента с переносом. [45] |
Страницы: 1 2 3 4