Свободный ион - кадмий
Cтраница 1
Свободные ионы кадмия, которые образуются при диссоциации комплекса по уравнению, приведенному на стр. [1]
Свободные ионы кадмия появляются в клетках как результат разложения металлотио-неина и инициируют новый синтез металлотионеина, связывающего кадмий и тем самым защищающего клетку от высокотоксичных свободных ионов кадмия. В случае, если трубчатые клетки обладают повышенной способностью к синтезу металлотионеина, могут возникать функциональные расстройства почек. [2]
Свободные ионы кадмия, которые образуются при диссоциации комплекса по уравнению, приведенному на стр. [3]
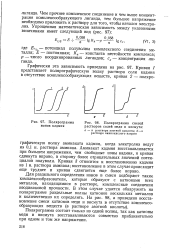 |
Полярограмма ионов кадмия.| Полярограмма смесей. [4] |
Аммиакат кадмия восстанавливается при большем напряжении, чем свободные ионы кадмия, и кривая сдвинута вправо, в сторону более отрицательных значений потенциалов полуволн. [5]
 |
Полярограмма комплек-соната кадмия в присутствии ионов циркония. [6] |
В результате реакции образуется комплекс циркония и освобождается эквивалентное количество свободных ионов кадмия. Появляется волна кадмия; измеряя высоту этой волны, можно вычислить концентрацию циркония в анализируемом растворе. [7]
Графически эта зависимость показана на рис. 25.9. Аммиакат кадмия восстанавливается при более отрицательном потенциале, чем свободные ионы кадмия, и кривая сдвинута вправо. Восстановление из 1 М раствора аммиака происходит в еще более отрицательной области потенциалов. [8]
От 80 до 90 % общего количества кадмия в организме, по-видимому, находится в связанном с металлотионеином состоянии, что предотвращает токсичное действие свободных ионов кадмия. Судя по всему, небольшие количества связанного с металлотионеином кадмия постоянно транспортируются с кровью из печени в почки. Металлотионеин, связанный с кадмием, отфильтровывается через гломерулы в первичную мочу. [9]
Свободные ионы кадмия появляются в клетках как результат разложения металлотио-неина и инициируют новый синтез металлотионеина, связывающего кадмий и тем самым защищающего клетку от высокотоксичных свободных ионов кадмия. В случае, если трубчатые клетки обладают повышенной способностью к синтезу металлотионеина, могут возникать функциональные расстройства почек. [10]
 |
Подпрограмма трилоната кадмия в присутствии ионов циркония. [11] |
В этом случае используют различные косвенные методы, основанные на неодинаковой прочности комплексных соединений металлов. Так, при определении циркония к анализируемому раствору прибавляют комплексонат кадмия ( этилендиаминтетраацетат кадмия); последний не восстанавливается при таком потенциале, который соответствует свободным ионом кадмия. Цирконий способен образовать этилендиаминтетраацетатный комплекс, значительно более прочный, чем соответствующий кадмиевый комплекс, поэтому между трилонатом кадмия и ионами циркония происходит обменная реакция, при которой образуется три-лонат циркония и освобождается эквивалентное количество свободных ионов кадмия. Теперь появляется волна кадмия; измеряя высоту этой волны, можно вычислить концентрацию циркония в анализируемом растворе. [12]
Сначала при рН 6 8 титруют кадмий раствором комплексона III, содержащим цинк, в присутствии индикатора солохром черного WDFA. T составляют 16 6 и 16 2 соответственно, а комплекс кадмия с солохром черным WDFA менее стоек, чем комплекс цинка с тем же индикатором. Свободные ионы кадмия замещают цинк в его комплексонате, освободившийся цинк в эквивалентной точке дает окрашенный комплекс с солохром черным VVDFA. Фактически индикатором является цинк в сочетании с солохром черным WDFA. Индикатор растворяют в смеси равных объемов триэтаноламииа и изопропаиола. [13]
Комплекс кадмия с этилендиаминтетрауксусной кислотой дает в умереннокислом растворе кинетическую полярографическую волну, образующуюся вследствие диссоциации комплекса. Эта волна в присутствии избытка этилендиаминтетрауксусной кислоты плохо измерима. Поэтому Танака и сотрудники [34] работали с избыточным количеством ионов кальция в полярогра-фируемом растворе, вследствие чего сдвигалось равновесие в растворе комплекса в сторону выделения свободного иона кадмия и кинетические токи значительно повышались. [14]
В этом случае используют различные косвенные методы, основанные на неодинаковой прочности комплексных соединений металлов. Так, при определении циркония к анализируемому раствору прибавляют комплексонат кадмия ( этилендиаминтетраацетат кадмия); последний не восстанавливается при таком потенциале, который соответствует свободным ионом кадмия. Цирконий способен образовать этилендиаминтетраацетатный комплекс, значительно более прочный, чем соответствующий кадмиевый комплекс, поэтому между трилонатом кадмия и ионами циркония происходит обменная реакция, при которой образуется три-лонат циркония и освобождается эквивалентное количество свободных ионов кадмия. Теперь появляется волна кадмия; измеряя высоту этой волны, можно вычислить концентрацию циркония в анализируемом растворе. [15]
Страницы: 1 2