Свободный ион - медь
Cтраница 1
Свободный ион меди находится в состоянии D. Это состояние под действием кубической компоненты электрического поля расщепляется на орбитальный дублет и триплет. Тетрагональная компонента поля и спин-орбитальное взаимодействие приводят к дальнейшему расщеплению на пять крамеровских дублетов, из которых занятым является только нижний. [1]
Свободный ион меди находится в состоянии ZD. Это состояние иод действием кубической компоненты электрического поля расщепляется на орбитальный дублет и триплет. Тетрагональная компонента поля и спин-орбитальное взаимодействие приводят к дальнейшему расщеплению на пять крамеровских дублетов, из которых занятым является только нижний. [2]
ПО ] концентрацию свободных ионов меди определяли с амальгамным медным электродом, а концентрацию свободных ионов водорода - со стеклянным электродом), систематически уменьшаются с увеличением числа протонов, входящих в состав отщепляющегося от комплекса лиганда. [3]
При разложении комплекса в организме образовавшиеся свободные ионы меди, независимо от того, с каким атомом ( хелатным узлом) они предварительно были связаны, должны были бы проявлять одинаковое действие. Однако экспериментальные данные свидетельствуют о другом. Так, три соединения меди: с пиколи-новой кислотой, ятреном и триэтилентетрамином, имеющие близкие по значению величины констант устойчивости, обладают резко различной кроветворной активностью; первые два почти совершенно неактивны, а третье проявляет значительную активность. [4]
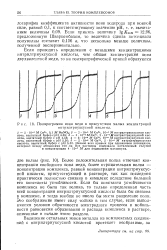 |
Подпрограмма иона меди в присутствии малых концентраций нитрилтриуксусной кислоты. [5] |
Более положительная волна отвечает концентрации свободного иона меди, более отрицательная волна - концентрации комплекса, равной концентрации нитрилтриуксусной кислоты, присутствующей в растворе, так как последняя практически полностью связана в комплекс вследствие большой его константы устойчивости. Если бы константа устойчивости комплекса не была так велика, то только определенная часть всей концентрации нитрилтриуксусной кислоты была бы связана в комплекс, и тогда вообще не имело бы места разделение волн. Это соображение имеет силу только в том случае, если выполняются условия обратимости электродного процесса и мобильности равновесия образования и распада комплекса в растворе, описанные в начале этого раздела. [6]
При титровании трилоном Б ( динатриевой солью ЭДТА) раствора, содержащего Си2 и индикатор, вначале связываются в этилендиаминтетраацетатный комплекс свободные ионы меди, а затем разрушаются комплексы меди с ПАР. Переход окраски раствора в зеленую ( это цвет свободного ПАР при рН 5) служит признаком конца титрования. [7]
Басоло и Пирсон4о считают более правдоподобным механизм, связанный со ступенчатой диссоциацией комплекса меди, сопровождаемой комплексообразованием отрывающегося ( или размыкающегося) циклического лиганда со свободным ионом меди. [8]
Басоло и Пирсон 4о считают более правдоподобным механизм, связанный со ступенчатой диссоциацией комплекса меди, сопровождаемой комплексообразованием отрывающегося ( или размыкающегося) циклического лиганда со свободным ионом меди. [9]
Например, щелочной раствор ЭДТА в присутствии люминола и Н2О2 титруют солью меди; сначала медь связывается в прочный комплекс с ЭДТА, а в точке эквивалентности свободные ионы меди начинают катализировать реакцию между люминолом и Н2О2 - появляется свечение раствора. [10]
Например, щелочной раствор ЭДТА в присутствии люми-нола и Н О2 титруют солью меди; сначала медь связывается в прочный комплекс с ЭДТА, а в точке эквивалентности свободные ионы меди начинают катализировать реакцию между люминолом и Н О2 - появляется свечение раствора. [11]
Они смешали раствор, содержащий большую концентрацию комплекса кадмия, с раствором, содержащим меньшую концентрацию медной соли, и при постоянном потенциале диффузионного тока полярографически регистрировали изменение во времени концентрации свободных ионов меди. [12]
Очевидно, что наличие Си-ионов, закрепленных на поверхности частиц, недостаточно для формирования пространственной структуры полигидроокиси и тем самым и структуры основного металлического мыла, образующейся на границе раздела фаз, при взаимодействии с поверхностно-активным модификатором. Стоит, однако, в эту суспензию ввести свободные ионы меди в виде разбавленного 0 01 7V раствора СиС12, как при том же значении рН7 образуется высокоустойчивая прямая эмульсия и межфазный слой приобретает исключительно высокую прочность. [13]
 |
Схемы строения защитных оболочек из частиц твердых эмульгаторов. [14] |
Очевидно, что наличие Си-ионов, закрепленных на поверхности частиц, недостаточно для формирования пространственной структуры полигидроокиси и тем самым и структуры основного металлического мыла, образующейся на границе раздела фаз, при взаимодействии с поверхностно-активным модификатором. Стоит, однако, в эту суспензию ввести свободные ионы меди в виде разбавленного 0 01 N раствора СиС12, как при том же значении рН7 образуется высокоустойчивая прямая эмульсия и межфазный слой приобретает исключительно высокую прочность. [15]
Страницы: 1 2