Карбонизующий газ
Cтраница 1
Карбонизующий газ, проходя через горячую зону, где начинается кристаллизация NaHCO3, нагревается и к выходу из колонны не успевает охладиться до температуры поступающего раствора. Нормами технологического режима температура выходящего газа предусмотрена 48 - 52 С. Снижение этой температуры говорит об опускании этой зоны ниже нормального уровня. Это обычно заставляет уменьшать отбор жидкости из колонны, и наоборот - при повышении температуры отходящего газа увеличивать отбор. [1]
Для поглощения углекислоты необходимо, чтобы давление СО2 в карбонизующем газе было больше давления СОа над раствором. По мере поглощения углекислоты давление СО2 над раствором увеличивается. Подача вниз осадительных колонн концентрированного газа ( газ 1-го ввода) позволяет получить раствор с более высокой степенью карбонизации и тем самым достичь более высокой степени использования натрия. Оставшуюся часть газа известковых печей подают компрессором 3 выше по колоннам 7 ( газ 2-го ввода), где жидкость менее прокарбонизована и концентрация СО2 в газе, идущем снизу по колонне, приближается к концентрации СО2 газа известковых печей. Подача части газа через 2 - й ввод, где сопротивление столба жидкости в колонне меньше, облегчает работу компрессора и снижает расход энергии. Кроме того, меньшее количество газа в нижней части колонны, где проходит густая суспензия, содержащая на выходе из колонны 30 % ( по весу) осажденного NaHCO3, снижает возможность подвисания колонны. [2]
Для поглощения двуокиси углерода необходимо, чтобы давление СОз в карбонизующем газе было больше давления СОг над раствором. [3]
Достижение максимально возможной степени карбонизации зависит от концентрации С02 в карбонизующем газе при прочих одинаковых условиях. Двуокись углерода поступает на карбонизацию из содовых и известковых печей. Газ из содовых печей, содержащий 85 - 90 % С02, идет на карбонизацию полностью. [4]
Для поглощения диоксида углерода необходимо, чтобы давление СО2 в карбонизующем газе было больше равновесного давления С02 над раствором. Газ известковых печей ( второй ввод) поступает в ту зону колонны, где содержание диоксида углерода в газе, идущем снизу, приближается к содержанию СО2 в газе второго ввода. Обычно второй ввод расположен выше холодильной зоны колонны. [5]
Достижение максимально возможной степени карбонизации зависит от концентрации С02 в карбонизующем газе при прочих одинаковых условиях. Двуокись углерода поступает на карбонизацию из содовых и известковых печей. Газ из содовых печей, содержащий 85 - 90 % С02, идет на карбонизацию полностью. [6]
Степень карбонизации в уравнении (1.7.6) зависит от содержания диоксида углерода в карбонизующем газе. Чем выше среднее содержание СС2, тем выше производительность карбонизационной колонны и, значит, тем меньше объем газа, проходящего через карбонизуемый раствор, что, в свою очередь, снижает выдувание аммиака и уменьшает расход энергии на транспортирование газа. [7]
Степень карбонизации К ( или количество поглощенной углекислоты) в уравнении ( 18) зависит от концентрации СО2 в карбонизующем газе. Углекислота на карбонизацию поступает из двух источников - из содовых и известковых печей. Газ из содовых печей, имеющий концентрацию СО2 около 85 - 90 %, забирают на карбонизацию полностью. [8]
Степень карбонизации R ( или количество поглощенной двуокиси углерода) в уравнении ( 18) зависит от концентрации СО2 в карбонизующем газе. Двуокись углерода на карбонизацию поступает из двух источников - из содовых и известковых печей. Газ из содовых печей с концентрацией СО2 около 85 - 90 % забирают на карбонизацию полностью. [9]
Так как в процессе карбонизации давление С02 над растворами зависит от состава растворов, то скорость абсорбции С02 должна зависеть от разности давлений СО2 в карбонизующем газе и над ме-тастабильным раствором. Таким образом, для выяснения кинетики процессов, протекающих - при карбонизации аммонизированного рас-сола, необходимо знать неравновесный состав раствора. [10]
Так как в процессе карбонизации давление СО 2 над растворами зависит от состава растворов, то скорость абсорбции С02 должна зависеть от разности давлений С02 в карбонизующем газе и над ме-тастабильным раствором. Таким образом, для выяснения кинетики процессов, протекающих при карбонизации аммонизированного рас - сола, необходимо знать неравновесный состав раствора. [11]
Из уравнения ( 18) видно, что количество NaHCOa, осажденного из производственных растворов, которые насыщены только бикарбонатом натрия, возрастает с по-нижение м температуры, так как при этом уменьшаются растворимость NaHCO3 и равновесное давление углекислоты над раствором, что позволяет поглотить больше углекислоты из карбонизующего газа и тем самым увеличить концентрацию NH4HCO3 в растворе. [12]
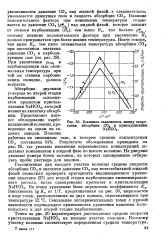 |
Взаимная зависимость между скора-абсорбции СО. и кристаллизации NaHCOs. [13] |
Rc): чем выше Rc, тем больше р о, поэтому влияние положительного фактора при увеличении Rc должно прекращаться при более низких температурах. При увеличении рсо, в карбонизующем газе оптимальная температура при той же степени карбонизации, очевидно, должна возрасти. [14]
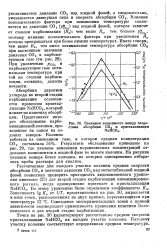 |
Взаимная зависимость между скоростями абсорбции СО. и кристаллизации NaHCOs. [15] |
Страницы: 1 2 3