Выделяющийся ион - водород
Cтраница 1
Выделяющиеся ионы водорода нейтрализуют. Для титрования применяют раствор нитратов тория и циркония, в которые вносят хинализарин и ализаринсульфонат натрия. [1]
 |
Схема установки для очистки воды ионно-обменными смолами. [2] |
Выделяющиеся ионы водорода совместно с анионами ( например, С1 -) поступают в колонку для анионитов. [3]
Выделяющиеся ионы водорода нейтрализуют. Для титрования применяют раствор нитратов тория и циркония, в которые вносят хинализарин и ализаринсульфонат натрия. [4]
В обоих случаях выделяющиеся ионы водорода медленно связываются уротропином или мочевиной, что приводит к постепенному сдвигу состояния равновесия приведенных реакций в правую сторону. [5]
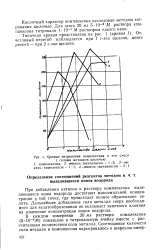 |
Кривые титрования комплексона и его смеси. [6] |
При добавлении катиона к раствору комплексона выделяющиеся ионы водорода достигают максимальной концентрации в той точке, где происходит полное образование хе-лата. Дальнейшее добавление соли металла сверх необходимого для хелатообразования не оказывает заметного влияния на изменение концентрации ионов водорода. [7]
Наличие щелочи способствует смещению равновесия вправо вследствие связывания выделяющихся ионов водорода в молекулы воды. [8]
Чтобы реакция комплексообразования шла до конца, нужно связать выделяющиеся ионы водорода. Поэтому при титровании к анализируемому раствору добавляют смесь хлорида и гидроксида аммония - аммиачный буфер. [9]
С этой целью был проведен ионный обмен в условиях, когда выделяющиеся ионы водорода поглощались анионитом в гидроксильной форме. Анионит ЭДЭ-10, совершенно не сорбирующий Str3 и обладающий большой скоростью обмена по отношению к сульфат-иону, оказался весьма подходящим средством для нейтрализации свободной кислоты. Эти кривые сорбции были получены как для полимеризацион-ных, так и для конденсационных катионитов. Прекращение сорбции Str3 во времени и весьма небольшие gstrs, поглощенные при рН 7, указывали на то, что мы имеем дело с квазиравновесными состояниями. Измельчение катионитов влечет за собой возрастание gstf ( рис. 6), что также подтверждает отсутствие равновесия в системе. [10]
Для более полного смещения реакции в сторону окисления мышьяковистой кислоты в мышьяковую выделяющиеся ионы водорода связывают гидрокарбонатом. [11]
Поэтому титруют в присутствии буферной смеси ( NH4OH NH4C1), которая нейтрализует кислотность от выделяющихся ионов водорода. [12]
Для полноты прот тсания реакции (13.12) ее проводят в растворе при рН - 7 в присутствии NaHCOs для связывания выделяющихся ионов водорода. Стандартные потенциалы пар 12 / 21 - ( 0 545 В) и As ( V) / As ( III) ( 0 56 В) очень близки, поэтому направление реакции (13.12) можно легко изменять путем изменения концентрации ионов водорода. [13]
Для полноты прот кания реакции (13.12) ее проводят в растворе при рН - 7 в присутствии NaHCOa для связывания выделяющихся ионов водорода. Стандартные потенциалы пар Ь / 21 - ( 0 545 В) и As ( V) / As ( III) ( 0 56 В) очень близки, поэтому направление реакции (13.12) можно легко изменять путем изменения концентрации ионов водорода. [14]
Индикатор хромоген черный специальный ЕТ 00 образует с Zn2 комплекс, окрашенный в фиолетово-красный цвет. Выделяющиеся ионы водорода должны быть нейтрализованы, поэтому определение рекомендуется производить в присутствии аммиачной буферной смеси с рН 10 ( приготовление ее, стр. [15]
Страницы: 1 2