Заряженный ион
Cтраница 4
В электролите 2 молекулы вещества диссоциируют на электрически заряженные ионы Na и СГ, а ионы растворителя - на ионы Н и ОБГ. Когда к металлическим электродам, погруженным в электролит, прикладывают разность потенциалов, положительно заряженные ионы ( катионы) движутся к катоду, а отрицательно заряженные ионы ( анионы) - к аноду, в результате электрическая цепь замыкается. При этом перенос электрических зарядов в металлических проводниках осуществляют электроны, а в электролите - ионы. Изменение носителей заряда в электрической цепи происходит на поверхности электродов, погруженных в электролит. [47]
Электрический ток может также возникнуть как результат движения заряженных ионов в жидкой среде. [48]
Ионофорез основан на неодинаковой подвижности в электрическом поле различно заряженных ионов. [49]
Растворитель, который находится в непосредственной близости к заряженному иону, обладает несколько другой диэлектрической проницаемостью, чем растворитель в целом. Это естественно, так как диэлектрическая проницаемость растворителя зависит от дипольного момента молекул, который под влиянием поля иона изменяется, а в связи с этим изменяется и диэлектрическая проницаемость. Под влиянием электролита структура жидкости и степень ассоциации молекул жидкости нарушаются, в связи с чем изменяется их диэлектрическая проницаемость. [50]
Растворитель, который находится в непосредственной близости к заряженному иону, обладает несколько другой диэлектрической проницаемостью, чем растворитель в целом. Это естественно, так как диэлектрическая проницаемость зависит от дипольного момента молекул растворителя. Дипольные мо менты под влиянием поля иона изменяются и в связи с этим изменяется и диэлектрическая проницаемость. [51]
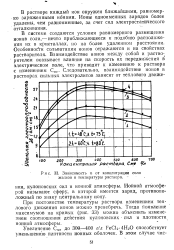 |
Зависимость х от концентрации соли железа и температуры раствора. [52] |
В растворе каждый ион окружен ближайшими, равномер-ко заряженными ионами. Ионы одноименных зарядов более удалены, чем разноименные, за счет сил электростатического отталкивания. [53]
Если не принимать во внимание проводимость, обусловленную диффузией заряженных ионов ( ионную проводимость), которая в исследуемых нами окислах вследствие ее крайне малой величины практически не играет роли, то единственной причиной электрического тока остается движение электронов. Во вводной главе с помощью анализа основных свойств зонного спектра электронов были объяснены причины большого различия значений проводимости в различных случаях; в металлах она очень велика, тогда как в диэлектриках, напротив, ею можно полностью пренебречь. [54]
А В - возникают осложнения, ибо при приближении заряженного иона к поверхности кристалла он может притягиваться ионами противоположного знака и одновременно отталкиваться ионами того же знака. [55]
Число атомов, смещенных в результате упругих соударений е быстрыми заряженными ионами, очень мало. Только после того как ион замедлится настолько, что потеряет свой заряд, упругие соударения станут существенными для потери энергии. Даже быстро движущиеся нейтральные атомы теряют значительную часть своей энергии на возбуждение электронной оболочки. [56]
Несложные опыты и рассуждения показывают, что разделение молекул на заряженные ионы не связано с наличием тока. Действительно, если бы молекулы разрывались внешним электрическим полем, то должна была бы существовать некоторая минимальная напряженность поля в электролите, необходимая для начала электролиза и зависящая от прочности молекул. Опыт же показывает, что это не так и что электролиз начинается при любом, сколь угодно малом поле. Это можно проверить, например, проводя электролиз медного купороса при медных электродах, когда нет искажающего влияния поляризации электродов ( § 77), какое бывает, например, при электролизе подкисленной воды. Подобного рода опыты показывают, что ионы возникают не под действием тока, а образуются в процессе растворения вещества. Образование ионов при растворении носит название электролитической диссоциации. [57]
Страницы: 1 2 3 4
