Отрицательно заряженный комплексный ион
Cтраница 1
Отрицательно заряженные комплексные ионы остаются в фильтрате. [1]
Использование комплексов металлов ( особенно отрицательно заряженных комплексных ионов) сильно расширяет возможности ионообменного разделения металлов. Большинство металлов в обычных водных растворах существует в виде катионов, разница в их сорбируемости катионитами сравнительно невелика, так что их разделение ограничено. При образовании отрицательно заряженных комплексных ионов или незаряженных комплексов металлов возможности разделения увеличиваются. [2]
Катионы, образующие с раствором электролита отрицательно заряженные комплексные ионы, проходят в фильтрат. Катионы, не образующие таких комплексных ионов, остаются на катионите. [3]
 |
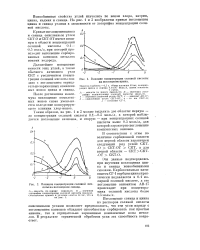
Влияние степени окисления на емкость угля СКТ по натрию ( 7, хлору ( 2, комплексным хлоридным ионам цинка ( 3 и кадмия ( 4. [4] |
Способность окисленного угля поглощать хлор-ионы и отрицательно заряженные комплексные ионы, по-видимому, объясняется частичным сохранением или образованием, кроме кислых, основных функциональных групп, отвечающих за сорбцию анионов. [5]
Катионы, образующие с раствором электролита отрицательно заряженные комплексные ионы, проходят в-фильтрат. Катионы, не образующие таких комплексных ионов, остаются на катионите. [6]
Катионы, образующие с раствором электролита отрицательно заряженные комплексные ионы, проходят в фильтрат. Катионы, не образующие таких комплексных ионов, остаются на катионите. [7]
Катионы, образующие с ( раствором электролита отрицательно заряженные комплексные ионы, проходят IB фильтрат. Катионы, не образующие отрицательно заряженных комплексных ионов, остаются на катионите. [8]
NaOH и уменьшается поглощение простых анионов и отрицательно заряженных комплексных ионов металлов. [9]
На ртутном капельном электроде могут восстанавливаться не только катионы, но и отрицательно заряженные комплексные ионы с атомом металла в центре [ например, Ре ( С2О4) з - ] во многих случаях восстановление таких частиц протекает обратимо. В этой главе рассматривается восстановление некоторых устойчивых анионов, образованных неметаллами, например IOg, BrOg, NOg, NO -, S 4O, -, S5Og - , S 2Og - , которое всегда протекает необратимо, и, кроме того, электродные процессы с участием анионов, содержащих металлы, которые также имеют необратимую электрохимическую стадию. [10]
На ртутном капельном электроде могут восстанавливаться не только катионы, но и отрицательно заряженные комплексные ионы с атомом металла в центре [ например, Ре ( С2О4) з - ]; во многих случаях восстановление таких частиц протекает обратимо. В этой главе рассматривается восстановление некоторых устойчиЕадх анионов, образованных неметаллами, например Ю, ВгО -, NO -, NOj, S4Oe -, S6Og, S2Og, которое всегда протекает необратимо, и, кроме того, электродные процессы с участием анионов, содержащих металлы, которые также имеют необратимую электрохимическую стадию. [11]
В ряде случаев подлежащие извлечению металлы содержатся в растворах в виде положительно или отрицательно заряженных комплексных ионов и могут быть удалены при помощи катионитов или анионитов. Иногда для извлечения металлов специально прибегают к образованию комплексных ионов. [12]
Кроме того, в сернокислом и карбонатном растворе уран может существовать в виде нейтральных или отрицательно заряженных комплексных ионов. Арден и Вуд [26] показали, что в разбавленных растворах уран присутствует в виде UO2 ( SO4) и что нейтральная молекула может быть легко захвачена сульфатом смолы. Для обработки кислых и щелочных растворов предпочитают использовать анионообменные смолы, так как они более избирательны для урана, чем катиониты. Принимая во внимание, что в растворе будут присутствовать катионы других металлов, наличие анионных и нейтральных комплексов урана позволяет провести на анионите эффективное отделение последнего от большинства металлов. Тот факт, что анионитная смола поглощает из раствора ион металла, конечно, не доказывает, что этот ион присутствует в виде анионного комплекса; стремление самой смолы к образованию анионных комплексов может быть достаточным условием, чтобы захватить металл. [13]
Разделение индия и цинка на анионите основано на том, что индий с тартратионами при рН 9 - 10 образует отрицательно заряженный комплексный ион [ 1п ( С4Н4С) б) 2р -, который сорбируется анионитом АН-2Ф в тартратной форме. Цинк в этих условиях образует положительно заряженный ион аммиаката цинка и проходит в Эффлюент. [14]
 |
Влияние концентрации соляпой кислоты на поглощение цинка.| Влияние концентрации соляной кислоты на поглощение свинца. [15] |
Страницы: 1 2 3