Отрицательно гидратированный ион
Cтраница 1
Отрицательно гидратированные ионы Cs разрыхляют структуру воды, тем самым облегчают переход молекул воды в поверхностный слой, адсорбция воды увеличивается, и поверхностное натяжение уменьшается. [1]
Механизм, согласно которому отрицательно гидратированные ионы повышают подвижность соседних молекул воды, относится к одному из самых неясных мест в явлениях сольватации. Были предложены три теоретические модели отрицательной гидратации. [2]
Поэтому оказывается термодинамически более выгодным переход отрицательно гидратированных ионов, разрушающих структуру воды, в ионит, а ионов с положительной гидратацией - во внешний раствор. [3]
В частности, по мнению Холма, сульфогруппа отрицательно гидратирована, вследствие чего сульфоиониты проявляют специфичность к отрицательно гидратированным ионам. [4]
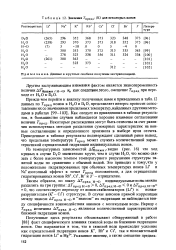 |
Значения Гпред ( К для некоторых ионов. [5] |
Из температурных зависимостей Д5бЛИЖН / видно ( рис. 16) что ход кривых в случае D2 О значительно круче, чем в случае Н2 О, что можно связать с более высоким темпом температурного разрушения структуры тяжелой воды по сравнению с обычной водой. Это приводит к тому, что у положительно гидратированных при обычных температурах ионов 1л и Na изотопный эффект в точке Тпреа положителен, а для отрицательно гидратированных ионов Rb, Cs, Br и J - отрицателен. [6]
Коэффициент В определяется взаимодействием ионов с растворителем, и величина его может быть как положительной, так и отрицательной в зависимости от свойств растворенного вещества и растворителя. Для водных растворов 1 - 1 электролитов, содержащих небольшие гидрофобные ионы, значения В обычно не превышают 0 2 л / моль; для солей с отрицательно гидратированными ионами В может принимать отрицательные значения: Й ( КС1, ag) - 0 014 л / моль, 5 ( CsNO3, ag) - 0 090 л / моль. Водные растворы электролитов с многовалентными или большими гидрофобными ионами, а также растворы солей в типичных неводных растворителях имеют сравнительно большие значения коэффи-циента В: B [ ( C4H9) H4NCl ag) 1 27 л / моль В ( КС1, DMSO) 0 80 л / моль. Необходимо отметить, что связь коэффициента В с различными макроскопическими параметрами широко используется для описания растворов электролитов. В работе [78] анализируется его связь с предельными кажущимися мольными объемами электролита: авторы [79] выводят уравнения, связывающие В с парциальными мольными объемами растворителя, электролита и с парциальными мольными свободными энтальпиями образования полости в растворе электролита и в растворителе. Наибольшее распространение для оценки ионных вкладов получили методы, основанные на электролитах сравнения, в качестве которых для водных растворов были использованы галогениды щелочных металлов, например, fi ( Rb) В ( Вг), а для неводных - iPe3BuNBPh4, Bu4NBPh4 и др. Однако получаемые результаты носят лишь оценочный характер, так как при этом исходят из предположения, что коэффициенты В характеризуют только взаимодействия ион-растворитель. [7]
Внимательное изучение рис. V.6 приводит к выводу, что положение кривых отдельных электролитов на них не случайное. Я - Самойлову [25] эти соли составлены отрицательно гидратированными ионами, а по Френку и Вину [247] они относятся к разряду структуроразрушаю-щих. На другом краю - соли лития, иона очень сильно гидратиро-ванного положительно по О. [8]
Солдатов и Старобинец [249, 250] изучили стандартные термодинамические функции обмена Ag - Н и Т1 - Н на сульфополи-стирольных катеонитах. Обмен иона таллия характеризуется большими отрицательными величинами АЯ и AS0, тогда как значения ДС почти одинаковы. Эти авторы предположили, что ионы таллия и серебра образуют ионные пары с сульфогруппой, однако в случае отрицательно гидратированного иона таллия образование ионной пары происходит без затраты энергии на дегидратацию. Отметим, что и для этих пар ионов также обнаружена описанная выше линейная зависимость ДЯ от Д5 для разных степеней сшивки. [9]
Они были рассчитаны на основе температурной зависимости эмпирических коэффициентов, входящих в уравнения для расчета энтропии одноатомных [1, 2] и многоатомных ионов [3] в водном растворе в интервале 0 - 100 С. Вычисленные по уравнению ( 2) величины ASn ( AS n) с повышением температуры уменьшаются. Для некоторых ионов при определенной температуре, характеризуемой условием А5ц 0 ( А5 ц 0), наблюдается знакопеременность указанных величин, объясняемая сменой гидратируемости иона. При этом отрицательно гидратированные ионы с повышением температуры при некотором ее предельном значении ( Т пред) [5] становятся положительно гидратироватаными. Для остальных ионов в интервале 0 - 100 С с повышением температуры увеличивается их положительная гидратируемость. [10]
Из анализа этих результатов можно заключить, что гидратные оболочки существуют вокруг каждого иона. Для молекул воды, сильно связанных в слое А, энергия EAEW, в то время как во второй гидратной оболочке В энергия слабо связанных с ионом молекул воды EBEW. Даже вокруг ионов, гидрати-рованных так же сильно, как Li, можно найти второй слой искаженной структуры. С другой стороны, вокруг больших отрицательно гидратированных ионов, например Cs, I - разд. В соответствии с этим вокруг каждого иона можно найти молекулы воды и с меньшей, и с большей подвижностью, чем в чистой воде. Если, однако, увеличение подвижности в слое В - преобладает, то наблюдается отрицательная гидратация. Согласно вычислениям величин ЕА и ЕВ, ионы Li и Na перемещаются с положительной гидратацией, в то время как ионы К, Cs, Cl - и 1 - обнаруживают отрицательную гидратацию. Для ионов с радиусом 1 13 А ЕА примерно равна Ев, они, так же как и ионы МОз, не изменяют средней подвижности молекул воды вокруг себя. Однако ионы С1О4 в соответствии с этими измерениями движутся с положительной гидратацией. Это указывает на то, что вокруг больших ионов структурные изменения в слое В обусловлены в основном электростатическим полем. Это поле возле каждого однозарядного иона одинаково зависит от расстояния. Вокруг небольших ионов молекулы воды в слое А расположены более компактно, чем в случае больших ионов. [11]
Страницы: 1