Безводный ион
Cтраница 1
Безводный ион Сп2 бесцветен, что подтверждается отсутствием окраски у безводного сульфата меди. [1]
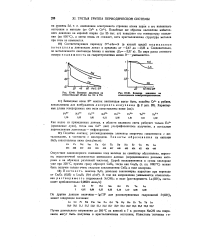 |
Влияние давления на относительный объем La, Се и Nd.| Влияние давлени m относительное электросопротивление. [2] |
Безводные ионы Э3 многих лантанидов могут быть, подобно Сг3 в рубине, использованы для возбуждения лазерного излучения ( § 2 доп. [3]
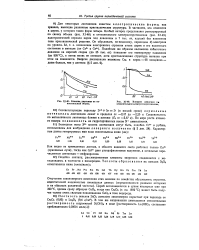 |
J-48. Влияние давленая на относительный объем.| Влияние давления не относительное электросопротивление. [4] |
Безводные ионы Э8 многих лантанидов могут быть, подобно Сга в рубине, использованы для возбуждения лазерного излучения ( § 2 доп. [5]
Соединения меди склонны к реакциям комплексообразования, Координационное число Си ( I) равно 2, а Си ( II), как правило, 4, Комплексообразованне проявляется даже в поведении ионов меди по отношению к воде. Безводный ион Си2 бесцветен, но растворение обезвоженных солей оксида меди ( II) в воде сопровождается образованием комплексных ионов [ Си ( Н2О) 4 ] ( Н20) 2 2, окрашенных в голубой цвет. Ионы меди могут образовывать комплексы с органическими лигандами. Соединение меди - гемоцианин играет у ракообразных ту же роль, что гемоглобин в крови высших животных. Медь входит в состав ряда ферментов, обеспечивающих перенос электронов в процессах окислительно-восстановительного цикла организма. [6]
ДК для безводной соли он оказывается не отрицательным, а положительным. Это означает прежде всего то, что весь эффект сжатия, наблюдаемый при растворении безводных ионов, приходится на счет образования координационной оболочки аквакомплекса. Однако было бы трудно предположить, что вводимые в воду ионы не производят никакого деструктурирования, во всяком случае в этом трудно заподозрить ионы СЮГ. Почему же тогда общий эффект оказывается положительным. Очевидно, вопреки деструктурирующе-му действию, приводящему к сжатию, имеется еще эффект или эффекты, вызывающие расширение. Мы полагаем, что в числе причин, могущих вызвать расширение, следует назвать взаимное отталкивание одноименно заряженных частиц и какое-либо взаимодействие, приводящее к образованию менее плотных структур из молекул воды, чем это имеет место в чистой воде. Полагая, что в общем случае могут действовать обе названные причины, мы склонны думать, что в разбавленных растворах первая из них играет второстепенную роль. [7]
Соли окиси железа могут быть легко получены окислением соответствующих солей закиси Fe. Большинство из них хорошо растворимо в воде. Так как основные свойства Fe ( OH) 3 выражены весьма слабо, соли трехвалентного железа в растворах подвергаются далеко идущему гидролизу. Образующиеся при этом основные соли придают растворам производных Fe3 характерную для них желто-коричневую окраску. Последняя не отвечает, та-ки образом, собственней окраске иона Fe, который ( равно как и безводный ион Fe3) сам по себе бесцветен. При добавлении избытка кислоты гидролиз ослабляется и окраска растворов бледнеет. [8]
Соли окиси железа могут быть получены окислением соответствующих солей закиси Fe. Большинство из них хорошо растворимо в воде. Так как основные свойства Fe ( OH) 3 выражены весьма слабо, соли трехвалентного железа в растворах подвергаются далеко идущему гидролизу. Образующиеся при этом основные соли придают растворам производных Fe3 характерную для них желто-коричневую окраску. Последняя не отвечает, таким образом, собственной окраске иона Fe % который ( равно как и безводный ион Fe3) сам по себе бесцветен. При добавлении избытка кислоты гидролиз ослабляется и окраска растворов бледнеет. [9]
Соли трехвалентного железа могут быть легко получены окислением соответствующих солей двухвалентного Fe. Большинство из них хорошо растворимо в воде. Так как основные свойства Fe ( OH) 3 выражены весьма слабо, соли трехвалентного железа в растворах подвергаются далеко идущему гидролизу. Образующиеся при этом основные соли придают растворам производных Fe3 характерную для них желто-коричневую окраску. Последняя не отвечает, таким образом, собственной окраске иона Ре, который ( равно как и безводный ион Fe3) сам по себе бесцветен. При добавлении избытка кислоты гидролиз ослабляется и окраска растворов бледнеет. [10]
Соли окиси железа могут быть получены окислением соответствующих солей закиси Fe. Большинство из них хорошо растворимо в воде. Так как основные свойства Fe ( OH) 3 выражены весьма слабо, соли трехвалентного железа в растворах подвергаются далеко идущему гидролизу. Образующиеся при этом основные соли придают растворам производных Fe3 характерную для них желто-коричневую окраску. Пр - - следняя не отвечает, таким образом, собственной окраске иона Fe, который ( равно как и безводный ион Fe3) сам по себе бесцветен. При добавлении избытка кислоты гидролиз ослабляется и окраска растворов бледнеет. [11]
Несмотря на многие неточности и неоднозначность, расчеты стоксовских радиусов полезны, поскольку они дают ценный ме - тод дифференциации сольватированных и несольватированных ионов. На основании этих данных было сделано заключение, что ионы натрия в отличие от ионов цезия сольватированы молекулами тетрагидрофурана. Аналогич-исследование растворов в диметоксиэтане [106] показывает, оба катиона сольватируются диметоксиэтаном. Однако на этот счет пока получено сравнительно Хмало сведений. Сильное взаимодействие между некоторыми ионами ( особенно ионами переходных металлов) и растворителем описывается на основе теории лигандов. Это взаимодействие может отражаться в значительных изменениях их электронных спектров. Например, безводные ионы двухвалентной меди бесцветны, тогда как гидратированные ионы окрашены в синий цвет. [12]
Страницы: 1