Отрицательный ион - фтор
Cтраница 1
Отрицательный ион одноатомного фтора в основном состоянии имеет электронную конфигурацию Is2 2s2 2pe, которой соответствует один терм JS. По аналогии с изо-электронным атомом Ne энергии перехода в возбужденные состояния иона F должны превышать 100 000 см-1. Поскольку потенциал ионизации F - существенно ниже этой величины ( см. стр. Это предположение находит подтверждение в неудаче попыток получить спектры отрицательно заряженных одноатомных ионов галогенов. [1]
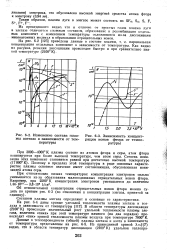 |
Изменение состава плаз.| Зависимость концент. [2] |
При относительно низких температурах концентрация электронов сильно уменьшается из-за образования малоподвижных отрицательных ионов фтора. [3]
Образование большого количества отрицательных ионов фтора при плавлении покрытия приводит к уменьшению проводимости дугового разряда и снижению устойчивости горения дуги. Поэтому сварку электродами с основным покрытием осуществляют на постоянном токе обратной полярности. [4]
Фтор является самым активным неметаллом и, следовательно, самым сильным окислителем. Никакой другой элемент не может отнимать электроны у отрицательных ионов фтора и превращать их в электронейтральные атомы. Поэтому свободный фтор получают только электролизом его соединений. [5]
Фтор является самым активным неметаллом и, следовательно, самым сильным окислителем. Никакой другой элемент не может отнимать электроны у отрицательных ионов фтора F и превращать их в электронейтральные атомы. [6]
Экспериментально доказано, что некоторые отрицательные ионы в парах энергетически устойчивы, хотя и очень реакционноспособ-ны. Наиболее тщательно исследованы атомы галогенов; например, чтобы оторвать электрон от отрицательного иона фтора, нужно затратить энергию, равную 81 ккал / моль. [8]
Большое влияние на величину напряжения зажигания оказывает эффективный потенциал ионизации. При наличии в дуговом промежутке паров легко ионизируемых элементов пик зажигания уменьшается. Отрицательные ионы фтора уменьшают степень ионизации дугового промежутка, что приводит к увеличению пика зажигания. [9]
Вышедшие из катода электроны, обладая весьма малой массой, проносятся в направлении к аноду с очень большой скоростью мимо положительных ионов, практически почти не соединяясь ( не реком-бинируя) с последними. Ионы фтора по своей массе соизмеримы с положительными ионами газа. Поэтому рекомбинация отрицательных ионов фтора с положительными ионами газа ( отдача электронов ионами фтора последним) в катодной области происходит во много раз больше ( по литературным данным в 104 раза), чем рекомбинация ( соединение) свободных электронов с положительными ионами. Уменьшение количества положительных ионов вследствие рекомбинации их с фтор-ионами приводит к повышению градиента потенциала в катодной области ( t / K) и в столбе дуги. В результате этого наряду с некоторой деионизацией и, следовательно, снижением стабильности горения дуги возрастает кинетическая энергия положительных ионов, бомбардирующих катод, вследствие чего соответственно повышаются выделение тепла на катоде и скорость его плавления. [10]
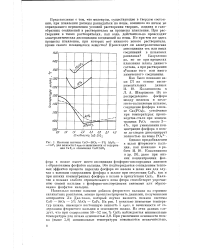 |
Изокомы системы CaO - SiC2 - 5 % AUOg - - CaFa для вязкости 5 пуаз в зависимости от содержания CaF2 и отношения CaO. Si02. [11] |
Однако при добавлении в шлак фтористого кальция, как показано в работе И. Ю. Кожевникова и др. [9], даже при низких концентрациях фосфора в шлаке имеет место ассоциация фосфорно-кислородных анионов с образованием фосфатов кальция. Это подтверждается совпадением тепловых эффектов процесса перехода фосфора из железа в шлак как для случая с высоким содержанием фосфора в шлаке при отсутствии CaF2, так и при низких концентрациях фосфора в шлаке в присутствии CaFa. Наличие в шлаках слабого отрицательного иона фтора способствует упрочнению связей кальция с фосфорно-кислородными анионами или образованию фосфатов кальция. [12]
Объяснение же состоит в следующем. При переходе от фтора к натрию заряд ядра увеличивается на две единицы, число электронов тоже увеличивается на два. Но одновременно начинается заполнение нового, третьего электронного уровня, а второй уровень, заполненный восемью электронами, оказывается внутренним по отношению к третьему. Электроны, находящиеся на втором уровне у фтора, экранируются от ядра лишь электронами первого уровня, по этой причине дополнительный электрон легко притягивается к ядру и образуется отрицательный ион фтора. [13]
Первая стадия требует затраты энергии 1 270 ккал, а последние две, как можно видеть из табл. 49 и 48, выделяют соответственно 1071 и 3 X 92, 1 276 ккал. Сродство иона алюминия к жидкой воде, обусловливающее вторую реакцию, меньше, чем его сродство к газообразному иону хлора, связанное с протеканием первой реакции; однако добавочная энергия гидратации иона хлора не только уравновешивает разницу, ной превышает ее. Кристаллический А1 ( Н20) еС13 при растворении выделяет лишь около 13 ккал. Интересно, что фтористый алюминий, вероятно, не является молекулярным кристаллом. Его структура более сложна и неправильна, причем каждый ион алюминия расположен среди ионов фтора, и строение соли, вероятно, близко к истинно ионному. Эта структура не является плотно упакованной, и известны гидраты состава отА1Р3 - 3 H - jO до AlFg - HsjO. Совершенно очевидно, что в этом кристалле структура молекулы воды не может играть такую же роль, как в других кристаллах, которые мы разбирали; молекулы воды примыкают лишь к отрицательным ионам фтора и совсем не подходят близко к положительным ионам. [14]
Страницы: 1