Избыточный ион
Cтраница 2
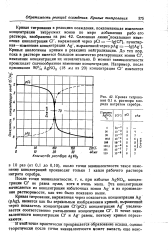 |
Кривая титрования 0 1 н. раствора хлорида нитратом серебра. [16] |
Эта концентрация вычисляется из концентрации избыточных ионов Ag и из произведения растворимости, как это было показано выше. [17]
Гидроксид-ионы связываются с катионом Zn2; избыточные ионы Н обусловливают кислую реакцию раствора. [18]
После точки эквивалентности в раствор вводятся избыточные ионы Ва2, образующие с ниг-хромазо синий комплекс. Поэтому после точки эквивалентности оптическая плотность раствора резко возрастает. [19]
 |
Схема установки для кулонометрического титрования. 7-аккумуляторная батарея. 2-реостат. 3-амперметр. i-ячейка. 5-анод. S - катод. 7-мешалка. [20] |
В этот момент в растворе появятся избыточные ионы железа ( II), которые обнаруживают колориметрическим способом по реакции с K3 [ Fe ( CN) ], потенциометрическим или полярографическим путями, о которых будет сказано в следующих главах. Количество электричества, израсходованного на восстановление железа и анализируемого хрома ( VI), в этом случае определяется временем электролиза, необходимым для появления избыточного железа ( II) в растворе. [21]
 |
Схема кулонометрического титрования. [22] |
В этот момент в растворе появятся избыточные ионы железа ( II), которые обнаруживают колориметрическим способом по реакции с K3 [ Fe ( CN) e ], потенциометр ическим или полярографическим путями, о которых будет сказано в следующих главах. Количество электричества, израсходованного на восстановление железа и анализируемого хрома ( VI), в этом случае определяется временем электролиза, необходимым для появления избыточного железа ( II) в растворе. [23]
 |
Кривые титрования. / - сильные электролиты. 2 - слабый полиэлектролит. [24] |
Аналогичным образом при добавлении сильной щелочи избыточные ионы ОН - реагируют с недиссоциированной кислотой с образованием воды и соответствующей соли. [25]
Сущность электроионитового метода состоит в удалении избыточных ионов посредством пропускания постоянного электрического тока через минерализованную воду, находящуюся между мембранами. [26]
Это означает, что появление одного избыточного иона О2 - связано с удалением одного иона Fe2 и образованием одного незамещенного узла ( дырки) в подрешетке железа. Иными словами в реальном вюстите не все октаэдрические пустоты в подрешетке кислорода заполнены ионами железа. Часть подобных междоузлий, статистически распределенная в кристалле [190], остается вакантной. [27]
Конечную точку находят по току восстановления избыточных ионов CeIV при потенциале 0 5 в платинового вращающегося электрода относительно насыщенного каломельного электрода. При титровании VIV в присутствии железа необходимо, чтобы часть последнего находилась в двухвалентном состоянии. В этом случае вначале титруют Fe п раствором Ce ( SO4) 2 при потенциале от 0 8 до 0 9 в, а затем V1V при потенциале 0 5 в. Метод используют для определения ванадия в феррохроме. [28]
Рассмотрим более подробно соединение электронов с избыточными ионами серебра. Применяя к этому процессу принцип Франка - Кондона, можно прийти к заключению о том, что вероятность соединения электронов с ионами серебра, адсорбированными на внешней поверхности, мала, так как в этом случае образованию атома серебра в основном состоянии должно предшествовать смещение ядер, вероятность которого близка к нулю. Для иона серебра, продиффундировавшего на границы субструктуры вдоль канала краевой дислокации, это ограничение отпадает. Такой ион находится в гораздо более симметричном поле диэлектрика, и, кроме того, в этом случае имеется пространство для образующегося атома серебра. Таким образом по внутренним границам субструктуры кристалла в непосредственной близости от поверхности образуется некоторое количество атомов серебра, химически эквивалентное количеству брома, выделившегося на поверхности. Когда ионы брома, расположенные на ступеньках вдоль линий дислокаций границ субструктуры, захватывают положительные дырки или, взаимодействуя с экситонами, образуют атомы брома, то возникающий одновременно с этим избыток ионов серебра будет иметь значительно большую вероятность соединения с электронами, чем ионы серебра на свободной поверхности. В этом случае соединение ионов серебра с электронами происходит быстрее, чем их удаление от атомов брома путем диффузии, и имеется большая вероятность для получающихся атомов серебра реагировать с атомами брома, образуя молекулы бромида серебра. [29]
 |
Изменение состава осадка в системе NIS04 - Li4 [ Fe ( CN6 ] - Н20.| Смешанные ферроцианиды никеля. [30] |
Страницы: 1 2 3 4