Одноатомный ион
Cтраница 2
Склонность к образованию одноатомных ионов с максимальной валентностью группы ( IV) очень мала и, естественно, возрастает у элементов с большими атомными номерами. Лишь олово и свинец образуют хорошо охарактеризованные четырехвалентные катионы, но и они могут существовать только в твердом состоянии; ионы С4 и Si4 неизвестны. С другой стороны, одноатомные четырехвалентные анионы С4 - образует только углерод в некоторых своих соединениях, причем эти анионы устойчивы лишь в твердом состоянии ( стр. Благодаря своему очень небольшому объему ( вследствие большого заряда ядра атома углерода его гелиевая оболочка сильно сжата) катион С4 не может существовать. Он настолько сильно деформировал бы анионы, с которыми соприкасался, что проникал бы в их электронные оболочки, образуя ковалентные связи. Это одна из важнейших причин, почему углерод проявляет исключительную склонность к образованию ковалентных связей. Эта склонность у других элементов IV группы выражена слабее и уменьшается с увеличением атомного номера. О неопределенности характера связи в соединениях более тяжелых элементов ( например, SnCl4 и РЬС14) - электровалентная или ковалентная - уже упоминалось на стр. [16]
Энтальпии образования некоторых одноатомных ионов при 298 15 К приводятся ниже. [17]
Поляризуемость атомов и одноатомных ионов, составляющих поверхностные слои твердого тела ( типа керамики), возрастает с увеличением числа электронов на внешней электронной оболочке. Одновременно изменяется равновесие положения частиц в поверхностном слое. Часть катионов несколько смещается внутрь материала, и поверхность приобретает заряд. Таким образом кристаллохимические свойства склеиваемого материала ( как и частицы связующего, наполнителя и новообразований) и электронное строение катионов влияют на смачиваемость и адгезию. С этих позиций повышение полярности материала должно, видимо, увеличивать адгезию. Следует учитывать, что начальная адгезия ( смачивание - прилипание с помощью жидкости) в неорганических клеях заменяется последующими прочными адгезионными контактами. [18]
Поскольку у большинства одноатомных ионов внешние валентные оболочки электронных орбиталей заполнены ( конфигурации благородных тазов), можно предположить, что такое же положение качественно будет иметь место и при отталкивании за счет перекрытия ионов. [19]
Известны трехвалентные и даже четырехвалентные одноатомные ионы, но способность элемента к их образованию и устойчивость этих ионов уменьшаются с увеличением диспропорции между зарядом ядра и соответственно дефицитом или избытком электронов в слое. У катионов по мере увеличения заряда ( и, следовательно, при уменьшении объема иона) возрастает способность элемента к образованию ковалентных соединений. Катионы с малым объемом и большим зарядом проникают глубоко в электронную оболочку аниона, что облегчает образование ковалентной связи. Явление хорошо наблюдается у соединений многовалентных металлов; например, галогениды металлов низших степеней валентности ( SnCl2, VC12, ТаС12) электровалентны, а галогениды металлов высших степеней валентности ( SnCl4, VC14) ковалентны. Зато известны многие устойчивые многоатомные анионы. [20]
Этого следовало ожидать для одноатомных ионов, так как правила строения атомов требуют, чтобы Sd-электроны оставались неспаренными до тех пор, пока не появляется необходимость спаривания. Это возникает впервые, когда число электронов достигает шести. Шестой должен занять одну из пяти Sd-орбит, образуя пару с другим электроном. Вычисленные значения спиновых моментов ( уравнение 16 - 3) сперва растут до максимального значения 5 92, отвечающего пяти неспаренным электронам, и затем, как показано в табл. 16, уменьшаются. [21]
Детальные термодинамические исследования сольватации одноатомных ионов Абросимова [686] позволили выяснить, как изменяется структура воды под влиянием ионов. Были получены соотношения для свободной энтальпии и изменений энтальпии, соответствующих переходу положительной, гидратации в отрицательную при возрастании размеров ионов. [22]
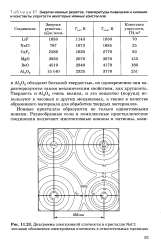 |
Диаграмма электронной плотности в кристалле NaCl. числами обозначена электронная плотность в относительных единицах. [23] |
Ионные кристаллы образуются не только одноатомными ионами. [24]
В соединениях, построенных из одноатомных ионов, эт ноны получают степени окисления, одинаковые с зарядом иона, соответственно положительные или отрицательные. [25]
В отличие от атомов и одноатомных ионов, обладающих энергетическими состояниями только одного типа, которые обусловлены движением электронов в электрическом поле ядра атома, энергетические состояния двухатомных молекул связаны с движением электронов в электрическом поле молекулы, с колебаниями ядер ее атомов друг относительно друга и с вращением ядер относительно центра тяжести молекулы. [26]
Степень окисления элемента в форме одноатомного иона в веществе, имеющем ионное строение, равна заряду этого иона. [27]
В соединениях, построенных из одноатомных ионов, эт ноны получают степени окисления, одинаковые с зарядом иона, соответственно положительные или отрицательные. [28]
 |
Схема образования воды.| Цикл Борна - Хабера. [29] |
Пусть процесс образования кристаллического вещества из одноатомных ионов может идти сразу, либо проходить через стадии образования сначала нейтральных атомов, а затем молекул. [30]
Страницы: 1 2 3 4