Трехвалентный ион
Cтраница 2
Возбуждение трехвалентных ионов осуществляется за счет переходов 4 / - - 4 /, интенсивность которых сравнительно мала. [16]
Гидроокиси трехвалентных ионов Al4 44, Ре 14 4, Cr 4 4 и Mn f осаждаются аммиаком и в присутствии солей аммония, потому что их константы произведения растворимости значительно меньше, чем у гидроокисей вышеуказанных двухвалентных металлов. Этим различием в свойствах пользуются для отделения А1, Сг и Fe ( III) от других металлов III группы. [17]
Окисление трехвалентных ионов хрома на аноде проходит с измеримой скоростью только на свинцовых анодах. На платиновых, стальных и железных анодах, в пределах 30 - 50 и плотностей тока на аноде 6 6 - 25 6 а / дм2, окисления трехвалентного хрома практически не наблюдается. [18]
Для трехвалентных ионов редких земель сравнение данных теории и опыта ( при Т 300) приведено в таблице. [19]
В кристаллах трехвалентные ионы изучены главным образом в соединениях LaCla и La ( C2H5SO4) 3 - 9H2O, широко применяемых при исследовании лантанидов. [20]
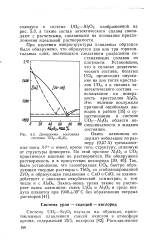 |
Диаграмма состояния Окись алюминия СО. [21] |
А) трехвалентные ионы А13 и имеет, кроме того, структуру, отличную от структуры флюорита. По этой причине А12О3 и 1Ю2 практически взаимно не растворяются. [22]
При электролизе трехвалентные ионы родия окисляются до большей валентности, что сопровождается изменением окраски раствора и ухудшением качества покрытий. Для торможения окислительного процесса анодная плотность тока должна быть в 2 - 3 раза ниже катодной. Эффективным средством является также изоляция анодного пространства керамическими диафрагмами. Таким путем при работе с электролитами, содержащими органические соединения, существенно ограничивается степень их окисления, что способствует увеличению срока эксплуатации раствора. [23]
Сггп обозначают промежуточный трехвалентный ион хрома и катионную вакансию в сульфиде хрома. Символы 0 и ф обозначают квази-свободный электрон в решетке и электронную дырку. Сульфид хрома является полупроводником р-типа с дефицитом металла и имеет катионные вакансии. [24]
 |
Магнитные свойства основных состоянии актиноидных ионов. [25] |
Магнитные свойства трехвалентных ионов очень похожи на свойства соответствующих ионов в группе 4 /, за исключением констант спин-орбитального взаимодействия, которые несколько больше. Они представляют собой линейные комплексы, в которых доминирует аксиальное взаимодействие с кислородом. Эти ионы аномальны в том смысле, что кристаллическое поле значительно сильнее спин-орбитального взаимодействия. Эти четыре электрона используются для образования ковалентных связей с атомами кислорода. [26]
Магнитная восприимчивость трехвалентных ионов в конденсированной фазе была измерена для всех лантаноидных элементов и для половины актиноидных. Их эффективные магнитные моменты приведены на рис. 3.30. У лантаноидных ионов экспериментально измеренные моменты находятся в соответствии с теоретическими значениями для i невозбужденного иона, рассчитанными из предположения, что рассел-саундерсовский тип связи распространяется на основное состояние электронных конфигураций и что это основное состояние подчиняется правилу Хунда. Моменты актиноидных ионов заметно хуже согласуются с теорией, несомненно, из-за более сильного взаимодействия / - электронов с кристаллическим полем и большей депрессии орбитального углового момента. [27]
Для серии трехвалентных ионов ( радиус Th3 определен из интерполяции) сжатие отвечает 0 08 А, что мало отличается от предыдущего значения. [28]
Различие адсорбируемости трехвалентных ионов хотя и невелико, однако оно представляет очень большой интерес в связи с разделением редкоземельных элементов ( см. статью Шуберта, стр. Рассел и Пирс [37], применяя алюмосиликатами конит, впервые показали, что это разделение возможно. Здесь мы имеем полную противоположность тому, что было найдено для щелочных и щелочноземельных металлов. [29]
 |
Микротрещины при электроосаждении хрома ( ХЮОО. [30] |
Страницы: 1 2 3 4