Трехвалентный ион - железо
Cтраница 1
Трехвалентный ион железа имеет 5 неспаренных электронов ( см. стр. Fe ( CN) e ] 3 -, у которого количество неспаренных электронов уменьшается до одного. Экспериментальным путем установлено, что магнитный момент этого иона равен 2 0, что удовлетворительно совпадает с результатом теоретического расчета. Таким образом, измерение магнитного момента подтверждает, что ион [ Fe ( CN) e ] 3 - образовался в результате с. [1]
Сорбоза восстанавливает трехвалентный ион железа в двухвалентный, а пирофосфат образует комплексы с железом в обоих его валентных состояних и поэтому уменьшает скорость реакции, протекающей с участием ионов железа. Так как органическая перекись растворима главным образом в участках, содержащих мономер, тогда как двухвалентное железо растворяется в большей мере в водной фазе, их взаимодействие снова замедляется. [2]
В присутствии трехвалентных ионов железа обрыв происходит путем восстановления ионов железа растущими цепями. [3]
В его состав входит трехвалентный ион железа; эта соль применяется для окисления сероводорода и других веществ, особенно в щелочных растворах. [4]
Электрон от диполя переходит на трехвалентный ион железа и переводит его в двухвалентный. [5]
Таким образом, двух - и трехвалентные ионы железа, мигрируя от положительных к отрицательным пластинам, могут перевести в сульфат значительное количество активной массы. [6]
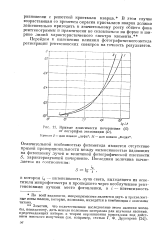 |
Кривые зависимости почернения ( S от логарифма экспозиции ( it. [7] |
По всей видимости, микропримесями являются двух-и трехвалентные ионы железа, которые, возможно, находятся в комбинации с окислами титана. [8]
Особо надо отметить роль железа в электролите: трехвалентные ионы железа взаимодействуют с металлической медью электродов и переводят ее в раствор по реакции 2Fes Си - 2Fe2 Cu2, что конечно крайне нежелательно. [9]
 |
Кристаллическая решетка Рез ( 4. [10] |
Его кристаллическая решетка - шпинель содержит двух - и трехвалентные ионы железа, расположенные в межузельных порах ионов кислорода. Два вида ионов железа и ионный тип связи обеспечивают оксиду особые магнитные свойства в высокочастотных полях. Большая плотность упаковки ионов в решетке, несмотря на небольшой дефицит ионов железа, способствует высокому сопротивлению химической коррозии. [11]
Близким по комплексообразуюшим свойствам к хрому является также и трехвалентный ион железа, Fe J. Механизмы взаимодействия ионов железа трехвалентного и алюминия трехвалентного с лмгносульфонатами аналогичны. Липшсульфонатные растворы, содержащие соли Fe 3 или A1 J, до 10 % масс, при термостатировании образуют рыхлые осадки. [12]
Близким по комплексообразующим свойствам к хрому является также и трехвалентный ион железа Ре 3, механизм взаимодействия которого с лигносульфонатами аналогичен хлориду алюминия. Лигносульфонатные 10 % - ные растворы, содержащие соли Ре 3 или А1 3, при термостатировании образуют рыхлые осадки. Экспериментально установлено, что оптимальная концетрация лигносульфонатов должна находиться в диапазоне 10 - 25 %, так как при низких концентрациях гель не образуется, а при высоких - слишком высока вязкость, которая затрудняет проведение технологического процесса. [13]
Примером зависимости саморазряда от примесей в электролите может служить действие двух - и трехвалентных ионов железа в аккумуляторной кислоте на положительные и отрицательные шгастины свинцовых аккумуляторов. [14]
Когда разделение ионов по длине колонки будет вполне ясным ( верхний слой бурый от трехвалентных ионов железа, средний - голубой от ионов меди, нижний бледно-фиолетовый, содержащий наиболее слабо адсорбирующиеся ионы двухвалентного кобальта), фильтрацию прекратить. [15]
Страницы: 1 2 3 4