Другие галоген
Cтраница 2
Действие других галогенов изучено хуже, но известно, что замещение хлором влияет на частоту карбонильного поглощения примерно в той же мере, как и замещение бромом. [16]
Для других галогенов такой широкий интервал концентраций не был исследован. К сожалению, промежуточная область, где можно было ожидать, применимости уравнения ( f), не была исследована. Возможно, что иод в этих реакциях ведет себя так же, как хлор, с той разницей, что кинетические выражения применимы в различных интервалах кислотности. [17]
Реакции других галогенов изучены в значительно меньшей степени. Однако интерпретация механизма, предлагаемая авторами, не учитывает влияния пористой структуры. [18]
Из других галогенов вольфрама интересен его гексафто-рид - WFe. Гексафторид вольфрама ( или шестифтористый вольфрам) представляет собой при нормальных условиях бесцветное газообразное вещество. Температура плавления гексафторида вольфрама составляет 2 5 С, температура кипения 19 5 С. [19]
Как и другие галогены, он достаточно активен - - непосредственно реагирует с большинством металлов ( даже благородное серебро устойчиво к действию йода лишь при температуре до 50 С), но уступает хлору и брому, не говоря уже о фторе. Некоторые элементы - углерод, азот, кислород, сера, селен - в непосредственную реакцию с йодом не вступают. [20]
 |
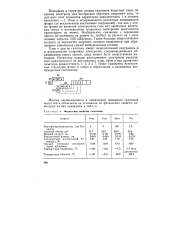
Допустимые концентрации серы ( в р. р. т для катализаторов паровой конверсии метана. [21] |
Хлор и другие галогены влияют аналогично сере, и для них допускаются приблизительно те же предельные концентрации. Как и в случае серы, их воздействие обратимо. [22]
Определению мешают другие галогены, галогеноводороды, синильная кислота и сероводород. [23]
Если же другие галогены присутствуют в олефине, то играет роль стерический фактор. [24]
Определению мешают другие галогены, галоидо-водороды и синильная кислота. [25]
 |
Физические свойства галогенов. [26] |
Хлор и другие галогены имеют незаполненный подуровень d и разъединение спаренных электронов, сопровождающееся образованием новых связей, здесь может быть энергетически выгодным. [27]
Хлор и другие галогены являются вредными примесями и действие их сравнимо с действием серы. Для них существуют такие же концентрационные ограничения. [28]
Как и другие галогены, он достаточно активен - непосредственно реагирует с большинством металлов ( даже благородное серебро устойчиво к действию иода лишь при температуре до 50 С), но уступает хлору и брому, не говоря уже о фторе. Некоторые элементы - углерод, азот, кислород, сера, селен - в непосредственную реакцию с иодом не вступают даже при высоких температурах. [29]
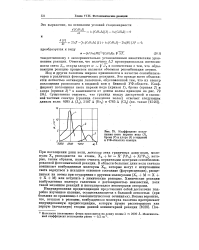 |
Коэффициент поглощения света парами иода ( 1, брома ( 2 и хлора ( 3 в видимой и УФ-областях спектра. [30] |
Страницы: 1 2 3 4