Газообразные галоген
Cтраница 1
Газообразные галогены вызывают появление цветов и пленок побежалости, тормозящих дальнейшую коррозию. Бром вызывает более сильную коррозию, чем хлор. Во влажном хлоре на холоду коррозия развивается сначала в соответствии с параболическим, а позднее - с линейным законом; объясняется это изменением механизма процесса. [1]
 |
Диаграмма, показывающая свойства полиэтиленовых серий. [2] |
Жидкие и газообразные галогены ( за исключением фтора) действуют на полиэтилен даже на холоду. Однако емкости из полиэтилена могут быть использованы для хранения плавиковой кислоты, которая действует на полиэтилен, как и фтор, при температуре выше 60 С. [3]
Особенно сильными окислительными свойствами обладают газообразные галогены. Многие химические элементы и вещества взаимодействуют с фтором и хлором уже при обычных условиях. В ряде случаев такое взаимодействие протекает очень бурно, с выделением большого количества тепла и может сопровождаться спеканием, плавлением или разбрызгиванием продуктов реакции. Для замедления этих реакций рекомендуется снижать давление газообразного галогена, добавлять к нему индифферентный газ или вводить в окисляемое вещество такой индифферентный наполнитель, как уголь. Продукты взаимодействия галогенов с неметаллами в условиях реакции часто переходят в газообразное или жидкое состояние. Это необходимо учитывать при синтезе. [4]
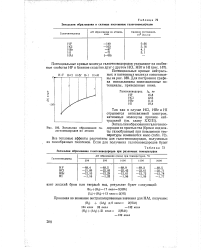 |
Энтальпии образования и силовые постоянные галогеноводородов.| Энтальпии образования галогеноводородов при различных температурах.| Энтальпии образования галогеноводородов из атомов. [5] |
Все тепловые эффекты рассчитаны для галогеноводородов, полученных из газообразных галогенов. [6]
 |
Связи в молекулах F2, и Вгг, представленные с помощью электронов Для удобства валентные Sd-электроны брома не указаны. [7] |
В табл. 19 - 1 приводятся также значения энергии ионизации атомов газообразных галогенов. Эти значения заметно уменьшаются при переходе от одного элемента к другому вниз по группе периодической таблицы. Следовательно, если какой-либо галоген реагирует со щелочным металлом, то образуется ионное твердое вещество. Такие ионные твердые вещества, или соли, содержат ионы галогенов F, С1 -, Вг - или I, электронные конфигурации которых соответствуют электронным конфигурациям инертных газов. [8]
Изучено влияние 32 ионов и найдено, что ионы Си, Tl ( III) и Bi ( III) влияют, газообразные галогены и органические вещества, растворимые в СС14, также влияют на определение ртути. Влияние рутения может быть устранено использованием гипохло-рита в качестве окислителя. [9]
Исследование примесей в газовых смесях, содержащих большие концентрации веществ, вызывающих коррозию, предъявляет жесткие требования к масс-спектрометру. В статье обсуждены некоторые особенности поведения газообразных галогенов и результаты, которые получаются при правильном выборе материалов и геометрии и при соответствующем проведении анализа. [10]
Газовый метод может осуществляться контактным ( его иногда называют способом порошков, поскольку диффундирующий элемент и остальные компоненты насыщающей смеси задаются в виде порошков) и неконтактным способами. При контактном способе газовая фаза генерируется в непосредственной близости от насыщаемой поверхности в результате взаимодействия частиц порошка диффундирующего элемента ( находящегося в свободном или связанном состоянии) с одним из газообразных галогенов или галоидных газов; при неконтактном - газовая фаза генерируется на значительном расстоянии от насыщаемого объекта и его поверхность не вступает в непосредственный контакт с диффундирующим элементом, находясь только в окружении чистой газовой фазы, которая содержит галогенид этого элемента. [11]
Это правило действует, когда между атомами образуются прочные химические связи. Например, атомы галогенов имеют 7 валентных электронов. Это справедливо не только для твердых и жидких, но и газообразных галогенов до тех пор, пока под влиянием высокой температуры молекулы не распадаются на атомы. Атомы кислорода, серы, селена и теллура имеют 6 валентных электронов. [12]
Кроме благородных газов, существует только одна группа элементов, которые находятся в газообразном состоянии в обычных лабораторных условиях - это элементы группы галогенов. Мы не будем рассматривать здесь астат, так как он не имеет устойчивых изотопов. Данные о реагирующих объемах, расчеты по методу Канниццаро, данные о теплоемкостях и многие другие факты свидетельствуют о том, что при обычных условиях элементы фтор, хлор, бром и иод представляют собой газы, состоящие из двухатомных молекул F2, C12, Вг2, Ь - В жидком и твердом состояниях эти элементы также состоят из двухатомных молекул. При высоких температурах двухатомные молекулы газообразных галогенов диссоциируют на атомы. Степень диссоциации при одинаковой температуре Т уменьшается от иода к брому и хлору, однако фтор диссоциирует почти так же, как и иод. [13]
Чтобы предотвратить образование гидратированной окиси рутения на трубке, соединяющей колбу с холодильником, нужно следить за температурой и скоростью пропускания воздуха через прибор. Некоторые затруднения могут возникнуть при выделении серы в результате реакции тиомочевины с попавшим в дистиллат окислителем. Поэтому не рекомендуется применять окислители, выделяющие газообразные галогены. Ниже приведен спектрофотометрический метод, предложенный Эрсом и Янгом [277] для анализа солянокислых дистиллатов, содержащих этанол. [14]
Страницы: 1