Галоген-ионы
Cтраница 2
Спектроскопическое исследование 70 комплексов сернистого ангидрида с С1 - -, Вг - - и 1 - - ионами показало, что все галогены усиливают электронный спектр сернистого ангидрида и вызывают бато-хромные сдвиги. Липпинкотт и Уэлч 80 идентифицировали комплексы 1 - - иона с сернистым ангидридом как комплексы с переходом заряда, и вполне резонно допустить, что такие комплексы с сернистым ангидридом могут образовывать все галоген-ионы. [16]
На практике необходима особая тщательность в отношении чистоты электрохимической ячейки. Следует избегать присутствия в электролите ионов ( случайных или каких-либо иных), способных образовывать комплексы с катионом металла электрода и, таким образом, вызывать коррозию электрода; особенно сильное действие, по-видимому, оказывают галоген-ионы. Другие электрохимически активные растворенные примеси ( например, растворенный кислород или катионы металлов) необходимо удалить. Для очистки растворов электролитов применяют три общих метода: пропускание через активный уголь, предварительный электролиз и использование вспомогательного ( сорбционного) электрода. К недостаткам предварительного электролиза относится возможность изменения поверхностных свойств исследуемого электрода; два других метода более предпочтительны. [17]
Таллий ( открытый Уильямом Круксом в 1886 г.) легко растворяется в азотной кислоте и несколько труднее - в серной кислоте, напоминая этим серебро. Оба соединения являются кристаллическими и бесцветными. Галоген-ионы с водными растворами этих солей образуют галоге-ниды одновалентного таллия T1CI, TlBr и ТП в виде нерастворимых творожистых осадков, напоминающих галогениды серебра. Они кристаллизуются в решетке иодида цезия ( стр. Хлорид таллия () бесцветен, бромид имеет желтоватую окраску, а иодид встречается в двух формах - желтой и красной. Фторид таллия T1F, как и фторид серебра, легко растворяется в воде. [18]
При адсорбции поверхностно-активных ионов работа ионизации водорода снижается, так как уменьшается прочность связи водорода с платиной. Снижение наклона кривых заряжения при переходе от SOi к С1 и Вг вызвано увеличением адсорбции галогенидов и соответствующим повышением емкости. В растворах, содержащих галоген-ионы, полные кривые заряжения получены быть не могут вследствие окисления анионов или их кислородсодержащих соединений. [19]
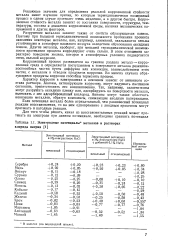 |
Электродные потенциалы металлов в растворах хлорида натрия. [20] |
Характер коррозии в электролитах в основном зависит от анионного состава раствора. Анионы, активирующие коррозию, могут нарушать пассивное состояние, препятствовать его возникновению. Так, например, галоген-ионы могут разрушать оксидную пленку или, адсорбируясь на поверхности металла, вытеснять с нее адсорбированный кислород. Анионы могут также облегчать ионизацию металлов, образуя комплексы, снижающие анодную поляризацию. [21]
Таким образом, в данном случае реакция, возможно, протекает на границе раздела фаз, минуя стадию образования ионной пары. Катион катализатора взаимодействует с - СС13, давая ионную пару, закрепленную на поверхности раздела фаз; при этом анион - СС13 находится в равновесии с карбеном ( стадия в), которое сдвинуто влево. В качестве акцепторов карбена могут быть уходящий С1 - или другие галоген-ионы, присутствующие в системе ( в этом случае можно обнаружить аддукты олефина со смешанным карбеном: СС1Х), вода, - ОН и олефин: они конкурируют друг с другом. [22]
Однако спектральные данные указывают на то, что связь в них подобна связи с переносом заряда. В разбавленных ( - 10 - 3 моль / л) растворах SO2 в воде, содержащих буфер с концентрацией 1 моль / л Н для подавления ионизации SO2, все галоген-ионы ( хлор, бром и иод) увеличивают Макс SO2, которая обычно находится при 276 ммк, и дают батохромные сдвиги, изменяющиеся в ряду I Вг - С1 -, причем в случае иод-иона полоса поглощения захватывает даже и часть видимой области. Кроме того, имеется даже большее изменение спектра в области коротких длин волн, максимум которого лежит ниже 200 ммк. [23]
Требуемые бутиндиолы легко получить конденсацией карбонильных соединений с ацетиленом. Восстановление бутиндиолов проводится дву-хлористым оловом в эфирном хлористом водороде или трехбромистым фосфором в пиридине. Вероятнее всего, галоген-ионы ускоряют образование дикарбониевого иона 133, который принимает два электрона ( освобождающиеся при реакции Sn ( II) - - Sn ( IV) - - 2е или Р ( III) - P ( V) 2е); а не два иона галогена. [24]
Требуемые бутиндиолы легко получить конденсацией карбонильных соединений с ацетиленом. Восстановление бутиндиолов проводится дву-хлористым оловом в эфирном хлористом водороде или трехбромистым фосфором в пиридине. Вероятнее всего, галоген-ионы ускоряют образование дикарбониевого иона 133, который принимает два электрона ( освобождающиеся при реакции Sn ( II) - - Sn ( IV) - f - 2е или Р ( III) - P ( V) 2e); а не два иона галогена. [25]
Для маскировки ионов металлов особенно широкое применение нашли такие лиганды, как ЭДТА, CN -, SCN - и др. Комплексы с ЭДТА отличаются высокой устойчивостью, растворимостью в воде; их образование можно регулировать путем изменения кислотности среды в соответствии с константами устойчивости ком-плексонатов. Цианид-ионы также образуют высокоустойчивые и растворимые в воде комплексы преимущественно с ионами металлов, проявляющими тенденцию к комплексообразованию с ли-гандами, содержащими атомы азота в качестве доноров. Очень высокой устойчивостью отличаются низкоспиновые цианидные комплексы ионов с заполненными или почти заполненными d - орбита-лями с высокой энергией стабилизации кристаллического поля. Эти же соображения в большой степени справедливы и для тио-цианатных комплексов. Наряду с этими лигандами успешно, применяются в качестве маскирующих реагентов некоторые гидрокси-карбоновые кислоты ( лимонная, винная), галоген-ионы ( F -, Cl -), амины ( аммиак, этилендиамин, триэтаноламин), серу - и фосфорсодержащие лиганды ( тиосульфат, тиокарбамид, фосфаты, фосфор-органические соединения) и др. Далее приведены некоторые характерные примеры использования маскирующих реагентов рассмотренных типов в различных видах количественного анализа. [26]
Страницы: 1 2