Галогениды - переходный металл
Cтраница 1
 |
Некоторые физические свойства нитрометана ( NM и нитробензола ( NB. [1] |
Галогениды переходных металлов обычно мало растворимы. [2]
Галогениды переходных металлов часто получают этим методом. [3]
Галогениды переходных металлов в высших степенях окисления являются ковалентными соединениями с молекулярной кристаллической решеткой, имеют низкие температуры плавления, растворяются в органических растворителях и легко гидролизуются водой. [4]
Исследуя галогениды переходных металлов, Тадмор [42-44] показал, что РеС13 и HgCl2 разделяются при 320 С на чистом трихлориде висмута, являющемся жидкой фазой, а галогениды олова хорошо отделяются друг от друга на силоиеле, покрытом А1Вг3, при 150 С. [6]
Так как примененные галогениды переходных металлов обычно неустойчивы, все эксперименты проводили в точно выбранных условиях для получения воспроизводимых результатов, подтверждающих устойчивость каталитических комплексов на протяжении всего процесса полимеризации. [7]
В отличие от окислов галогениды переходных металлов проявляют значительно меньшую тенденцию к отклонениям от октаэдри-ческой координации ионов металлов. Явным исключением являются галогениды меди ( 1), в которых ион Си окружен тетраэдром из галогенов. Дифториды переходных элементов от Сг до Zn сходны с MgF2 в том, что они имеют структуру рутила. Однако в отличие от Mg2 у многих ионов переходных металлов наблюдаются искажения октаэдрической координации. Наиболее существенное искажение обнаружено для Си2 и Сг2, у которых два расстояния М - F значительно длиннее ( примерно на 20 %), чем остальные четыре расстояния, так что координацию можно описать как псевдоплоскую квадратную. Многие другие дигалогениды имеют структуры, основанные на плотноупакованных решетках галогенов с половиной занятых октаэдрических дырок. Так, в МпС12, FeCl2, СоС12, № С12, Nil3 и ZnBr2 галогенидная решетка представляет собой кубическую плотную упаковку, а в MnI2, FeBr2, FeI2, CoBr2, CoI2 и № Вг2 имеется гексагональная плотная упаковка галогенов. Многие тригалогениды сходны с дигалогенидами в том отношении, что они также основаны на плотных упаковках галогенов с катионами металлов в октаэдрических дырках. В этих случаях стехиометри-ческие соотношения требуют, чтобы была заполнена одна треть дырок. Следует отметить, что в ZnQ2 ионы цинка находятся в тетраэдрическом окружении. [8]
При действии C5H5Na на галогениды переходных металлов обычно образуются бис-я-циклопент адиенильные соединения. Связь С5НБ - М в этих комплексах носит ионный характер. [9]
Особенности взаимодействия в системах галогенид переходного металла - мак-роциклический лиганд / Н. С. Ениколопян, А. М. Бочкин, А. Д. Помогайло и др. / / Докл. [10]
Натта считает, что металлоорганическое соединение и галогенид переходного металла образуют мостиковый комплекс. [11]
Газохроматографическим методом могут быть разделены и количественно определены галогениды переходных металлов. [12]
Полагают, что эти сокатализаторы служат лишь для того, чтобы алкилировать галогенид переходного металла. [13]
Молекулярный вес полипропилена и полибутена-1, полученных в присутствии каталитической системы триалкилалюминий - галогенид переходного металла, зависит от соотношения компонентов катализатора. [14]
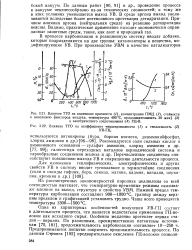 |
Влияние ТТО на изменение прочности ( /, концентрации ПЛЩ ( 2, стойкости. [15] |
Страницы: 1 2