Галогениды - щелочноземельный металл
Cтраница 1
Галогениды щелочноземельных металлов будут иметь заполненные пи - и л - орбитали и формально свободные d - орбитали. Фи, весьма возможно, что возбуждение ( я) - ( 8g) происходит легко и вызывает изгиб молекулы. Только Са, Sr и Ва имеют в своей валентной оболочке свободные d - op - битали, и они тогда должны обладать низшими энергиями возбуждения. Отметим, что смешивание 1яи - и 8г - орбиталей эквивалентно образованию pd - гибридных орбиталей. [1]
Галогениды щелочноземельных металлов по свойствам делятся на две довольно резко обособленные группы. К одной относятся фториды, к другой - производные остальных галогенов. Фториды почти нерастворимы не только в воде, но и в разбавленных кислотах. Кристаллогидраты для них неизвестны. Хлориды, бромиды и иодиды хорошо растворимы в воде и из растворов выделяются в виде кристаллогидратов. [2]
Галогениды щелочноземельных металлов по своим свойствам делятся на две довольно резко обособленные группы. К одной относятся фториды, к другой - производные остальных галоидов. [3]
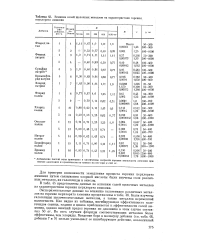 |
Влияние солей щелочных металлов на характеристики горения перхлората аммония. [4] |
Были изучены галогениды щелочноземельных металлов, а также металлов переменной валентности. Как видно из таблицы, ингибирующая эффективность галогенидов свинца, кадмия и цинка приближается к эффективности солей аммония, однако нижний предел горения по давлению в этом случае составлял 50 ат. Во всех случаях фториды соответствующих металлов более эффективны, чем хлориды. [5]
Позднее, когда для обнаружения молекул, обладающих постоянным дипольным моментом, стал применяться метод отклонения молекулярных пучков в неоднородном электрическом поле, было установлено, что некоторые галогениды щелочноземельных металлов имеют постоянный дипольный момент. [6]
Имеющиеся к настоящему времени работы посвящены в основном измерению энтальпий растворения щелочных галогенидов, и лишь в очень небольшой степени исследовались другие соли, в частности перхлораты и галогениды щелочноземельных металлов. Все использованные в различных работах растворители ( их около двадцати) можно разделить на несколько групп. К третьей группе относятся слирты и большая часть других органических жидкостей, жидкий аммиак. [7]
По-видимому, чисто ионная модель для молекулы СаС12 оправдывает себя в меньшей степени, чем в случае галогенидов щелочных металлов. Вообще галогениды щелочноземельных металлов обладают значительно более ковалентным характером, чем галогениды щелочных металлов. [8]
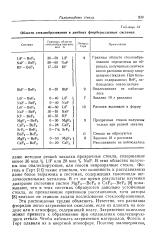 |
Области стеклообразования в двойных фторбериллатных системах. [9] |
В этих областях получены или опалесцирующие, или совсем непрозрачные стекла. Фо-гель и Герт [11] также отметили, что склонность к расслаиванию даже более выражена в системах, содержащих галогениды щелочноземельных металлов. В то же время результаты изучения диаграмм состояния систем MgF2 - BeF2 и CaF2 - BeF2 [8] показывают, что в этих системах образуются довольно устойчивые стекла, не проявляющие признаков расслаивания, хотя авторы [8] вначале не ставили задачи исследования стеклообразования. Эти расхождения трудно объяснить. Известно, что расплавы фторидов легко загрязняются окислами, если их плавить на воздухе или в атмосфере, содержащей влагу. Загрязнение окислами может привести к образованию при охлаждении опалесцирую-щего стекла. Чтобы избежать загрязнения материалов, Фогель и Герт плавили их в инертной атмосфере. [10]
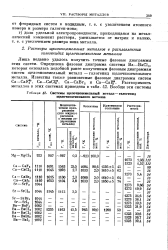 |
Системы щелочноземельный металл-галогенид щелочноземельного металла. [11] |
Лишь недавно удалось получить точные фазовые диаграммы этих систем. Определена фазовая диаграмма системы Ва - ВаС12, которая оказалась подобной ранее полученным фазовым диаграммам систем щелочноземельный металл - галогенид щелочноземельного металла. [12]
Хлорид лития гигроскопичен в отличие от галогенидов остальных щелочных металлов, которые не поглощают влагу воздуха. Это свойство также не встречается у галогенидов остальных щелочных металлов. Этим они похожи на галогениды щелочноземельных металлов. Наконец, LiCl растворяется в спирте и в других кислородсодержащих органических соединениях. [13]
В работах [223-226] показано, что щелочные металлы способны внедряться в решетку. То, что щелочные и щелочноземельные металлы часто встречаются в концентрациях от 10 - 4 до 10 - 2 ат. В [229] проведены измерения на легированных Na кристаллах CdS, содержащих 2 X X Ю-3 мол. Предполагается [224], что На и Li в ZnS действуют как активаторы при наличии галогенида и как отравляющие центры в его отсутствие. Li в кристаллах ZnS, отожженных при 1200 в атмосфере H2S, более растворим, чем Na, a KC1 и галогениды щелочноземельных металлов вообще не оказывают никакого влияния на свойства. Li в CdTe [232] создает акцепторный уровень. [14]
Страницы: 1