Галогениды - неметалл
Cтраница 1
Галогениды неметаллов - чаще всего жидкие или газообразные соединения с ковалентным типом связей. [1]
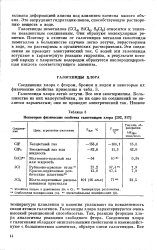 |
Некоторые физические свойства галогенидов хлора. [2] |
Галогениды неметаллов ( СС14, SiCl4, S2C12) относятся к типично ковалентным соединениям. Они образуют молекулярные решетки. Поэтому в отличие от галогенидов металлов галогениды неметаллов в большинстве случаев легко летучи, нерастворимы в воде, но растворимы в органических растворителях. Эти соединения не проводят электрический ток. С водой эти галогениды вступают в характерную реакцию гидролиза, в результате которой наряду с хлористым водородом образуется кислородсодержащая кислота соответствующего элемента. [3]
Многие галогениды неметаллов растворимы в броме. Образование в этих растворах соединений пока не доказано. Трихлорид фосфора растворяется в броме с образованием хлорбромидов. [4]
Гидролиз галогенидов неметаллов и металлов протекает различным образом. Галогениды неметаллов образуют при гидролизе смесь двух кислот: галогеноводородной и оксокислоты неметалла. [5]
К другому типу галогенидов - галогенидам неметаллов - относятся типичные ковалентные соединения. Поэтому галогениды неметаллов представляют собой летучие вещества, часто газообразные или жидкие при комнатной температуре, нерастворимые в воде, но растворимые в органических жидкостях. Эти соединения не проводят электрический ток. Их растворы не содержат галоген-ионов и, следовательно, не осаждают ионы серебра, однако с водой эти галогениды вступают в характерную реакцию гидролиза ( гидролиз РС13 обсуждался на стр. [6]
К катализаторам - галоидным металлам относятся хлористый и бромистый алюминий, хлорное железо, хлористый цинк, хлорное олово, четыреххлористый титан и другие галогениды группы, известной под названием катализаторов Фриделя - Крафтса. Фтористый бор, галогенид неметалла, имеет активность, подобную активности хлористого алюминия. [7]
Подавляющее большинство химических реакций протекает в водных или неводных растворах. Химики-органики чаще используют неполярные растворители, например тетрахлорид углерода и бензол, а химики-неорганики применяют, помимо воды, такие полярные растворители, как аммиак, серная и уксусная кислоты, диоксид серы, галогениды неметаллов. [8]
 |
Некоторые свойства германия, олова и свинца. [9] |
Проявляемая данными элементами высшая степень окисления 4 отвечает участию в образовании связей всех электронов внешнего слоя. Основной характер оксидов и гидроксидов усиливается с ростом радиусов ионов Э2; из оксидов данных элементов наиболее кислотный GeO2, а наиболее основной РЬО. Соединения ЭГ4 похожи на галогениды неметаллов, а ЭГ2, особенно РЬГ2, - соли. [10]
 |
Некоторые свойства германия, олова и свинца. [11] |
Проявляемая данными элементами высшая степень окисления 4 отвечает участию в образовании связей всех 1 - и / - электронов. Основной характер оксидов и гидроксидов усиливается с ростом радиусов ионов Э2; из оксидов данных элементов наиболее кислотный GeOi, а наиболее основные свойства выражены у РЬО. Соединения ЭГ похожи на галогениды неметаллов, а ЭГг, особенно PbPj, - соли. [12]
 |
Некоторые свойства германия, олова и свинца. [13] |
Прояв-ляемая данными элементами высшая степень окисления 4 отве чает участию в образовании связей всех электронов внешнего слоя. Основной характер оксидов и гидроксидов усиливается с ростом радиусов ионов Э2; из оксидов данных элементов наиболее кислотный GeO2, а наиболее основной РЬО. Соединения ЭГ4 похожи на галогениды неметаллов, а ЭГг, особенно РЬГ2, - соли. [14]
 |
Некоторые свойства германия, олова и свинца. [15] |
Страницы: 1 2